Ciklopropán
| Ciklopropán[1] | |||
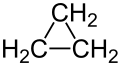 |

| ||

| |||
| IUPAC-név | Ciklopropán | ||
| Kémiai azonosítók | |||
|---|---|---|---|
| CAS-szám | 75-19-4 | ||
| |||
| Kémiai és fizikai tulajdonságok | |||
| Kémiai képlet | C3H6 | ||
| Moláris tömeg | 42,08 g/mol | ||
| Sűrűség | 1,879 g/L (1 atm, 0 °C) | ||
| Olvadáspont | -128 °C | ||
| Forráspont | -33 °C | ||
| Veszélyek | |||
| EU osztályozás | Fokozottan tűzveszélyes (F+)[2] | ||
| R mondatok | R12[2] | ||
| S mondatok | (S2), S9, S16, S33[2] | ||
| Ha másként nem jelöljük, az adatok az anyag standardállapotára (100 kPa) és 25 °C-os hőmérsékletre vonatkoznak. | |||
A ciklopropán (C3H6) a cikloalkánok közé tartozó szerves vegyület, melyben három szénatom gyűrűt alkotva kapcsolódik egymáshoz, valamint egyenként két hidrogénatomhoz. A legegyszerűbb cikloalkán. Színtelen, dietil-éterre emlékeztető szagú, kábító, narkotikus hatású gáz. 1,3-diklórpropánból állítható elő cinkkel, nátrium-jodid jelenlétében. Ez a reakció egy módosított Wurtz-szintézisnek fogható fel. A szénatomok közötti kötések jóval gyengébbek, mint egy átlagos kovalens kötés. Ezt a 60°-os szög okozza, amely jóval az átlagos 109,5°-os szög alatt van (sp3 hibridizált molekulapályák). Azonban feszültsége azért csak kevéssel nagyobb, mint a ciklobutáné (27,6 kJ/mol és 26,4 kJ/mol), mert σ-aromás jelleget mutattak ki nála.
Ez a szög-feszültség levonódik a kötési energiából, ezért a vegyület reaktívabb az alkánoknál és más cikloalkánoknál (ciklopentán, ciklohexán, cikloheptán) is. A természetben nagy reakciókészsége miatt nem fordul elő.
Kémiai reakciói szerkesztés
A ciklopropán kémiai tulajdonságai inkább az alkének, mint az alkánok kémiai tulajdonságaira emlékeztetnek. Brómmal a nyílt láncú alkánoktól eltérően addíciós, és nem szubsztitúciós reakcióba lép. Az addíció a gyűrű felnyílásával jár, nyílt láncú 1,3-dibrómpropán keletkezik. A brómhoz hasonlóan addícionál hidrogén-jodidot és hidrogént is. Megvilágítás hatására klórral azonban szubsztitúciós reakcióba lép. Katalizátor jelenlétében vagy hő hatására a gyűrűje felnyílik, propilénné alakul.
Jegyzetek szerkesztés
- ↑ Merck Index, 11th Edition, 2755.
- ↑ a b c A ciklopropán (ESIS)[halott link]