Langerhans-sejt
A Langerhans-sejtek a bőrben található specializált dendritikus sejtek (az immunrendszerhez tartozó antigénprezentáló sejtek). Az epidermisz valamennyi rétegében előfordulnak, de legnagyobb mennyiségben a stratum spinosum-ban találhatók meg.[1] Ezenkívül előfordulnak a dermisz papilláris rétegében, különösen a vérerek körül,[1] valamint a száj nyálkahártyájában, a fityma és a hüvely epitéliumában.[2] Szabályozatlan szaporodásuk egy ritka tumoros megbetegedést, a Langerhans-sejtes hisztiocitózist okozhat.

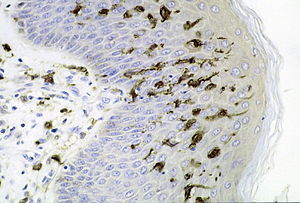
Nevüket Paul Langerhans 19. századi német fiziológusról kapták, aki 21 évesen fedezte fel, és dendritikus kinövéseik miatt tévesen az idegrendszerhez sorolta őket.
Feladata
szerkesztésA Langerhans-sejtek a bőr és nyálkahártya szöveteiben felismerik a kórokozó mikroorganizmusokat, bekebelezik őket és feldolgozott antigénjeiket prezentálják a felületükön. A folyamat közben a sejtek érett dendritikus sejtté válnak, amelyek a másodlagos nyirokszervekbe vándorolnak és képesek lesznek aktiválni a naiv T-limfocitákat, amellyel felkészítik az immunrendszert az adott kórokozó elleni küzdelemre.
A Langerhans-sejtek olyan csontvelőbeli elődsejtekből származnak, amelyek a eredetileg a terhesség első trimeszterében alakulnak ki a szikzacskó primitív makrofágjaiból, amelyek később az embrió bőrszövetébe kerülnek és normál esetben egész életen át megmaradnak és osztódásukkal Langerhans-sejteket produkálnak. Szükség esetén, pl. fertőzés okozta súlyos bőrgyulladás során a vérből monociták érkeznek a helyszínre és ők is Langerhans-sejtekké differenciálódhatnak; vagyis ilyen esetben a sejtpopuláció kettős eredetű.[3]
A Langerhans-sejtekre jellemző a langerin molekula (transzmembrán c-típusú lektin protein) termelése és az ún. Birbeck-granulumok jelenléte a citoplazmában[4][5]
Klinikai jelentősége
szerkesztésLangerhans-sejtes hisztiocitózis
szerkesztésA ritka Langerhans-sejtes hisztiocitózis esetén nagy mennyiségű ilyen jellegű sejt jelenléte figyelhető meg a csontban vagy egyéb szövetekben. Immunhisztokémiai módszerekkel azonban kimutatták, hogy sok szempontból különböznek az eredeti Langerhans-sejtektől, például a monocitákra jellemző CD14 marker található rajtuk és eredetük is inkább a vérképző szervek felé mutat.[6] A betegség a bőr, csont és egyéb szervek szöveteit károsítja.
HIV
szerkesztésA nemi szervek nyálkahártyájában található Langerhans-sejtek a HIV-fertőzés első célpontjai között lehetnek.[7] a későbbiekben pedig vírusrezervoárok, vagy a fertőzés nyirokrendszeren belüli elterjesztésének eszközei lehetnek.[8] A felszínükön található langerin viszont a jelek szerint gátolja a vírusfertőzést.[9]
Elképzelhető a száj nyálkahártyájának érintettsége is, de itt kisebb a Langerhans-sejtek száma a nemi szervek epitéliumához képest és így szerepük feltehetőleg nem számottevő.[2]
HPV
szerkesztésA méhnyakrákos eseteknek több mint a felét a humán papillómavírus-16 (HPV16) okozza.[10] A vírus életciklusa során az epitélium bazális sejtjeit fertőzi meg és kapcsolatba kerül a környező Langerhans-sejtekkel.[11] Sejttenyészetes kísérletekben a HPV nem aktiválta a Langerhans-sejteket; lehetséges hogy a vírus ezáltal kerüli ki a szervezet immunválaszát.[12] Kimutatták, hogy a Langerhans-sejtekbe bekerülő vírus képes blokkolni annak szignáljait és megakadályozza az érett sejtté való átalakulását.[13] Ez a mechanizmus, ami lehetővé teszi az immunrendszer előli elrejtőzést (kivéve ha gyulladás is fellép), a jelek szerint a legtöbb HPV-törzsnél megtalálható.[14] Azt is kimutatták, hogy az inativált Langerhans-sejtekkel kapcsolatba kerülő T-sejtek nem defektesek, a későbbiekben megfelelő stimulusra maguk is aktiválhatóak.[15]
A HPV-okozta méhnyakléziókban található Langerhans-sejtek lekerekítettek, hiányoznak a dendritjeik és szupresszív hatású interleukin-10-et választanak ki.[16]
Jegyzetek
szerkesztés- ↑ a b Wheater's Functional Histology, 4th, Churchill Livingstone, 162. o. (2000). ISBN 0-443-05612-9
- ↑ a b (1995) „Comparative investigation of Langerhans' cells and potential receptors for HIV in oral, genitourinary and rectal epithelia”. Immunology 85 (3), 475–84. o. PMID 7558138.
- ↑ (2016) „Langerhans cell origin and regulation”. Current Opinion in Hematology 23 (1), 28–35. o. DOI:10.1097/MOH.0000000000000202.
- ↑ (2003) „Langerin/CD207 Sheds Light on Formation of Birbeck Granules and Their Possible Function in Langerhans Cells”. Immunologic Research 28 (2), 93–107. o. DOI:10.1385/IR:28:2:93. PMID 14610287.
- ↑ (2007) „The dermis contains langerin+ dendritic cells that develop and function independently of epidermal Langerhans cells”. Journal of Experimental Medicine 204 (13), 3119–31. o. [2018. július 19-i dátummal az eredetiből archiválva]. DOI:10.1084/jem.20071724. PMID 18086861. (Hozzáférés: 2018. november 23.)
- ↑ NCI Summary View > Urology - Yale School of Medicine. medicine.yale.edu . [2019. június 17-i dátummal az eredetiből archiválva]. (Hozzáférés: 2018. április 19.)
- ↑ (2005) „The role of Langerhans cells in the sexual transmission of HIV”. Journal of Dermatological Science 40 (3), 147–55. o. DOI:10.1016/j.jdermsci.2005.08.009. PMID 16226431.
- ↑ (1995. december 1.) „Cellules dendritiques épithéliales et infection par HIV-1 in vivo et in vitro” (french nyelven). Pathologie Biologie 43 (10), 882–8. o. PMID 8786894.
- ↑ (2007) „Langerin is a natural barrier to HIV-1 transmission by Langerhans cells”. Nature Medicine 13 (3), 367–71. o. DOI:10.1038/nm1541. PMID 17334373.
- ↑ Bosch, F. X. (1995. június 7.). „Prevalence of human papillomavirus in cervical cancer: a worldwide perspective. International biological study on cervical cancer (IBSCC) Study Group”. Journal of the National Cancer Institute 87 (11), 796–802. o. DOI:10.1093/jnci/87.11.796. ISSN 0027-8874. PMID 7791229.
- ↑ Stanley, M. A. (2007. december 1.). „HPV: from infection to cancer”. Biochemical Society Transactions 35 (Pt 6), 1456–1460. o. DOI:10.1042/BST0351456. ISSN 0300-5127. PMID 18031245.
- ↑ Fausch, Steven C. (2002. szeptember 15.). „Human papillomavirus virus-like particles do not activate Langerhans cells: a possible immune escape mechanism used by human papillomaviruses”. Journal of Immunology 169 (6), 3242–3249. o. DOI:10.4049/jimmunol.169.6.3242. ISSN 0022-1767. PMID 12218143.
- ↑ Woodham, Andrew W. (2014. május 15.). „Inhibition of Langerhans cell maturation by human papillomavirus type 16: a novel role for the annexin A2 heterotetramer in immune suppression”. Journal of Immunology 192 (10), 4748–4757. o. DOI:10.4049/jimmunol.1303190. ISSN 1550-6606. PMID 24719459.
- ↑ Da Silva, Diane M. (2014. március 1.). „Suppression of Langerhans cell activation is conserved amongst human papillomavirus α and β genotypes, but not a µ genotype”. Virology 452-453, 279–286. o. DOI:10.1016/j.virol.2014.01.031. ISSN 1096-0341. PMID 24606705.
- ↑ Woodham, Andrew W. (2016. december 1.). „T cell ignorance is bliss: T cells are not tolerized by Langerhans cells presenting human papillomavirus antigens in the absence of costimulation”. Papillomavirus Research (Amsterdam, Netherlands) 2, 21–30. o. DOI:10.1016/j.pvr.2016.01.002. ISSN 2405-8521. PMID 27182559.
- ↑ Prata, Thiago Theodoro Martins (2015. szeptember 1.). „Local immunosuppression induced by high viral load of human papillomavirus: characterization of cellular phenotypes producing interleukin-10 in cervical neoplastic lesions”. Immunology 146 (1), 113–121. o. DOI:10.1111/imm.12487. ISSN 1365-2567. PMID 26059395.
Fordítás
szerkesztés- Ez a szócikk részben vagy egészben a Langerhans cell című angol Wikipédia-szócikk ezen változatának fordításán alapul. Az eredeti cikk szerkesztőit annak laptörténete sorolja fel. Ez a jelzés csupán a megfogalmazás eredetét és a szerzői jogokat jelzi, nem szolgál a cikkben szereplő információk forrásmegjelöléseként.