Paklitaxel
A paklitaxel (kereskedelmi néven Taxol) egy tumorellenes szer, amelyet számos daganatos kórképben alkalmaznak, köztük Kaposi-szarkómában, petefészek-, emlő-, tüdő-, méhnyak- és hasnyálmirigyrákban. Általában intravénásan történik a beadása, és albuminhoz kötött formulációja is forgalomban van.[2]
| |||

| |||
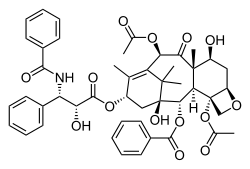
| Paklitaxel | |||
| IUPAC-név | |||
| (2α,4α,5β,7β,10β,13α)-4,10-Bisz(acetiloxi)-13-{[(2R,3S)-3-(benzoilamino)-2-hidroxi-3-fenilpropanoil]oxi}-1,7-dihidroxi-9-oxo-5,20-epoxitax-11-én-2-il benzoát | |||
| Kémiai azonosítók | |||
| CAS-szám | 33069-62-4 | ||
| PubChem | 36314 | ||
| ChemSpider | 10368587 | ||
| DrugBank | DB01229 | ||
| KEGG | D00491 | ||
| ChEBI | 45863 | ||
| ATC kód | L01CD01, L01CD03 (paclitaxel poliglumex) | ||
| |||
| InChIKey | RCINICONZNJXQF-MZXODVADSA-N | ||
| UNII | P88XT4IS4D | ||
| ChEMBL | 428647 | ||
| Kémiai és fizikai tulajdonságok | |||
| Kémiai képlet | C47H51NO14 | ||
| Moláris tömeg | 853,906 g/mol | ||
| Farmakokinetikai adatok | |||
| Biohasznosíthatóság | 6,5% (per os)[1] | ||
| Metabolizmus | [Máj (CYP2C8 és CYP3A4) | ||
| Biológiai felezési idő |
5,8 óra | ||
| Fehérjekötés | 89–98% | ||
| Kiválasztás | Széklet és vizelet | ||
| Terápiás előírások | |||
| Licenc adat | igen (EU) | ||
| Jogi státusz | Rx-only | ||
| S4 | |||
| POM | |||
| Rx-only | |||
| Terhességi kategória | D (US) | ||
| Alkalmazás | Intravénás | ||
Gyakori mellékhatásai közé tartozik a hajhullás, csontvelő-szupresszió, zsibbadás, allergiás reakciók, izomfájdalom és hasmenés. Egyéb súlyos mellékhatásai is megjelenhetnek, többek között szívproblémák, csökkent ellenállóképesség fertőzésekkel szemben és tüdőgyulladás.[2] Terhesség idején alkalmazása abszolút ellenjavalt, mert születési rendellenességeket okozhat.[2][3]
A paklitaxel a taxánok közé tartozó diterpén-pszeudoalkaloid[4] (pontosabban proto pszeudoalkaloid, mivel a nitrogénatom nem a gyűrűben, hanem az oldalláncban található).[5] Hatását a sejtosztódás során fejti ki, a mikrotubuláris rendszer működésének megzavarásával.[2]
1971-ben izolálták először az amerikai tiszafa (Taxus brevifolia) kérgéből, és 1993-ban engedélyezték gyógyászati alkalmazását.[6][7] Szerepel az Egészségügyi Világszervezet (WHO) Model List of Essential Medicines listáján, a leghatékonyabb és legbiztonságosabb gyógyszerek között.[8] Nagykereskedelmi ára: 7,06–13,48 USD/100 mg körül mozog világszerte, míg az Egyesült Királyságban 66,85 font.[9][10] Előállítása manapság biotechnológiai úton, sejttenyészetek segítségével történik.[7]
Orvosi alkalmazása
szerkesztésA paklitaxel az Egyesült Királyságban petefészek-, emlő-, tüdő-, hólyag- és nyelőcsőrákban, melanómában valamint más szolid tumorokban, mint például Kaposi-szarkómában engedélyezett gyógyszer.[11] Magyarországon emlőrák, petefészekrák, nem kissejtes tüdőrák, és Kaposi-szarkóma esetén alkalmazható szer.[12][13]
Az angliai Egészség és Klinikai Kiválóság Nemzeti Intézete (National Institute for Health and Care Excellence, NICE) 2001. júniusi irányelve alapján olyan nem kissejtes tüdőkarcinómás (NSCLC) betegek kezelésében ajánlott a paklitaxel, akiknél nem végezhető kuratív terápia, továbbá a paklitaxel alkalmazható a petefészek-daganat első és második vonalbeli kezelésében. 2001 szeptemberében a NICE egy újabb állásfoglalásában a paklitaxelt olyan előrehaladott emlőkarcinómában szenvedő betegeknél is javasolja, akiknél az antraciklin terápia hatástalannak bizonyult, azonban első vonalbeli alkalmazását csak klinikai vizsgálatokra engedélyezné az intézet. 2006 szeptemberében kiadott ajánlásában a NICE nem javasolja a paklitaxelt nyirokcsomó-pozitív emlődaganatos betegek kiegészítő terápiájában.[14] Az Amerikai Egyesült Államokban 2018-ban mell-, hasnyálmirigy-, petefészek- és nem kissejtes tüdőrák, továbbá Kaposi-szarkóma kezelésére engedélyezték.[15][16]
Hasonló szerek
szerkesztésAz albuminhoz kötött paklitaxel (nab-paklitaxel néven is ismert; kereskedelmi néven Abraxane) egy olyan készítmény, amelyben a paklitaxel albuminhoz kötött nanorészecskés formulában található. A paklitaxel klinikai toxicitásáért a Cremophor EL-t teszik felelőssé, melyet segédanyagként alkalmaznak a paklitaxel feloldására.[17] Ezt szerette volna kiküszöbölni az Abraxis BioScience az Abraxane kifejlesztésével. Az FDA 2005 januárjában engedélyezte az Abraxane-t olyan emlőrákban szenvedő betegnél, akiknél a kombinációs kemoterápia hatástalan volt, vagy hat hónapon belül visszaestek a kiegészítő kemoterápia után.[18] Azóta engedélyezték lokálisan előrehaladott vagy áttétes kissejtes tüdőkarcinómában illetve áttétes hasnyálmirigy adenokarcinómában.[19]
A paklitaxel különböző szintézisutainak kifejlesztése vezetett a docetaxelhez. A docetaxel (kereskedelmi néven Taxotere) a paklitaxelhez hasonló terápiás indikációkkal rendelkezik, azonban kötődési affinitása közel kétszer akkora, mint a paklitaxelnek, ezért terápiás dózisa alacsonyabb.[20]
Egy 2008-as tanulmány alapján számos taxán, köztük a paklitaxel, 10-dezaceti-lbaccatin III, baccatin III, paklitaxel C és 7-epipaklitaxel megtalálható a közönséges mogyoró (Corylus avellana) levelében és termésének héjában.[21] A mogyoróhéj az élelmiszeriparban nagy mennyiségben keletkező melléktermék, s ez a felfedezés hozzájárulhat a paklitaxel ezen alternatív forrásból való kinyerésének kifejlesztéséhez.
Restenosis (stentbeültetést követő újbóli érszűkület)
szerkesztésA paklitaxelt sejtosztódásgátlóként alkalmazzák koronária és perifériás stentek esetén jelentkező restenosis megelőzésére.[22] A paklitaxelt a stent felületére kötve lokálisan juttatják az artéria falára, amely csökkenti a neointima (hegszövet) kialakulását. Paklitaxel tartalmú gyógyszerkibocsátó stentet az USA-ban Taxus néven hoztak forgalomba.
Mellékhatások
szerkesztésA paklitaxel gyakori mellékhatásai közé tartozik: allergiás reakciók (enyhébb esetben kipirulás, viszketés, bőrkiütés, súlyosabb esetben mellkasi szorítás, légszomj, nehézlégzés, duzzanatok), csontvelő-szupresszió, mely következtében csökken a fertőző betegségekkel szembeni ellenállás, hajhullás, izom- és ízületi fájdalmak, perifériás neuropátia (végtagok zsibbadása és bizsergése). Jelentkezhet még hányinger, hányás, hasmenés és a vér alakos elemeinek számbeli csökkenése (anémia, trombocitopénia). Kevésbé gyakori a köröm- és bőrelváltozások, illetve szívproblémák megjelenése. Az intravénás injekció helyén lokális tünetek is jelentkezhetnek.[12][13]
Az allergiás reakciók egy része összefüggésbe hozható a Cremophor EL segédanyaggal, amely polioxietilált ricinusolaj. Azoknál a betegek, akik allergiásak ciklosporinra, tenipozidra és más polioxietilált ricinusolaj tartalmú gyógyszerekre, fokozott a kockázata a mellékhatások megjelenésének.[23]
Hatásmechanizmus
szerkesztésA paklitaxel a sejtváz integritására ható szerek közé tartozik, és támadáspontja a mikrotubulusokat alkotó β-tubulin,[24] amelyen a taxán kötőhelyhez kapcsolódik. Hatására gátlódik az osztódási orsók összeszerelődése, testvérkromatidák szétválása, és így maga a sejtosztódás is. Eltérően más mikrotubulus-ellenes szerektől, mint például a mikrotubulusok polimerizációját megakadályozó kolchicintől, a paklitaxel stabilizálja a kialakult mikrotubulus polimert, és nem engedi annak szétszerelődését. Így a testvérkromatidák nem válnak szét, és a sejtciklus leáll. A mitózis blokádja és a mitotikus ellenőrzési pont elnyúlása apoptózist idéz elő, vagy pedig a sejt G0 fázisba áll vissza a sejt kettéosztódása nélkül.[25][26]
A paklitaxel gátló hatását a mikrotubulusok dinamikus átszerveződésének megakadályozásával hozzák kapcsolatba,[27] de más tanulmányok alapján a dinamikus átszerveződés gátlása már olyan alacsonyabb paklitaxel-koncentrációknál is megjelenik, amely koncentrációk még nem gátolják magát a mitózist. Magasabb terápiás koncentrációban a paklitaxel gátolja a mikrotubulus leválását a centroszómákról, ami normálisan a mitózis során lejátszódik.[28]
Előállítás
szerkesztésKéregfeldolgozás
szerkesztésA paklitaxelt 1967–1993 között szinte teljes mértékben az amerikai tiszafa kérgéből állították elő. A kéreg eltávolításával járó kinyerési folyamatot a fa nem éli túl.[29] Az eredeti eljárást Monroe Wall és Mansukh Wani dolgozta ki. 1987-ben az amerikai Nemzeti Rákkutató Intézet (National Cancer Institute, NCI) a coloradói Hauser Chemical Research-t bízta meg klinikai vizsgálatok II-es és III-as fázisához elegendő mennyiségű hatóanyag előállításával. Mind az amerikai tiszafa természetes populációjának, mind a végső paklitaxel igényének mérete kérdéses volt, s rövidesen világossá vált, hogy új alternatív és fenntartható források után kell nézni. A kezdeti természetes források keresése során megvizsgálták az amerikai tiszafa levelét, majd más vad és nemesített Taxus fajok tartalomanyagait is, de ezek a próbálkozások alacsony és gyakran nagyon változó kitermeléssel jártak. Az 1990-es évek elejére az északnyugat-amerikai erdők ökológiailag érzékennyé váltak, míg a paklitaxel kinyerésének mértéke épp ekkor érte el azt a szintet, amely kielégítette a klinikai vizsgálatok hatóanyagigényét.[30]
Félszintetikus előállítás
szerkesztésAmerikai és francia szerves kémikusokat már az 1970-es évek óta foglalkoztatta a paklitaxel szintetikus előállítása. 1992-ben nagy erőkkel dolgoztak a paklitaxel totálszintézisén, de mindezt nem a nagyipari előállítás motiválta, hanem jóval inkább a kémiai tudásvágy. Pierre Potier kutatócsoportja a francia Nemzeti Tudományos Kutatási Központban (Centre national de la recherche scientifique, CNRS) foglalkozott a teljes kinyerés hozamával, majd megvizsgálva a CNRS kampuszából származó közönséges tiszafa (Taxus baccata) tűlevelét azt találták, hogy az viszonylag nagyobb mennyiségű 10‑dezacetilbaccatint tartalmaz. A 10‑dezacetil-baccatin szerkezete alapján úgy tűnt, hogy csupán néhány kémiai módosítással paklitaxellé alakítható. 1988-ban Potier és munkatársai publikálták is ezen félszintetikus eljárást.[31]
Az NCI szemszögéből ez az eljárás még mindig nem volt a gyakorlatban hasznosítható eljárás. Robert A. Holton kutatócsoportja szintén kidolgozott egy félszintézist, ami már a Potier-féle szintézis hozamának a dupláját tudta biztosítani. A Florida State University, ahol Holton dolgozott, megállapodást kötött a Bristol-Myers Squibb (BMS) amerikai gyógyszergyárral a félszintetikus útvonal levédéséről és egy jövőbeli szabadalomról. Holton 1992-ben védette le az optimalizált 80%-os hozamú folyamatot, amit a BMS saját részre hasznosított, és el is kezdte Írországban a paklitaxel gyártását az európai tiszafa tűleveléből kinyert 10‑dezacetil-baccatinből. A BMS 1993-ban jelentette be, hogy az amerikai tiszafa kérgének feldolgozását 1995-re szüntetik meg, amivel ténylegesen megoldódott az amerikai tiszafa túlzott kitermelésével járó környezetvédelmi kérdés. Így sikerült eleget tennie azon elköteleződésének, hogy alternatív előállítási útvonalak felé tereli a termelést, amit az NCI egy az amerikai kormány és a magánvállalatok közötti együttműködésben (CRADA) vállalt.
2013-ig a BMS a közönséges tiszafa tűleveléből történő félszintetikus eljárással állította elő a paklitaxelt,[32] míg a céggel 2012-ig együtt dolgozó Phyton Biotech Inc. növényi sejtes fermentációs technológiával állítja elő.[33][34] Egy specifikus Taxus sejtvonal tartályokban való fermentációjával feleslegessé válik a különböző tiszafák felhasználása.[35] A paklitaxel így egy szuszpenzióból nyerhető ki, amely közel 40%-os hatóanyag tartalmú port eredményez. Ezt egy kromatográfiás tisztítás, majd pedig egy kristályosítás követ.[36] A félszintetikus eljáráshoz képest a fermentációs technológia kevesebb veszélyes vegyszert igényel, és kevesebb energiafelhasználással is jár.[37]
1993-ban a paklitaxelt egy tiszafában élő endofita gombából is kimutatták.[38] Azóta a következő endofita gombákról derült ki ugyanez: Nodulisporium sylviforme,[39] Alternaria taxi, Cladosporium cladosporioides MD2, Metarhizium anisopliae, Aspergillus candidus MD3, Mucor rouxianus, Chaetomella raphigera, Phyllosticta tabernaemontanae, Phomopsis, Pestalotiopsis pauciseta, Phyllosticta citricarpa, Podocarpus sp., Fusarium solani, Pestalotiopsis terminaliae, Pestalotiopsis breviseta, Botryodiplodia theobromae, Gliocladium sp., Alternaria alternata var. monosporus, Cladosporium cladosporioides, Nigrospora sp., Pestalotiopsis versicolor és Taxomyces andreanae. Mindazonáltal ellentmondásos eredmények születtek arról, hogy vajon az endofiták termelik-e a paklitaxelt.[40][41]
Bioszintézis
szerkesztésBioszintézise egy terpenoid útvonalon keresztül valósul meg, amely egy részét sikeresen megvalósítottak E. Coli[42] és élesztőgombában is.[43]
Totálszintézis
szerkesztés1992-re világszerte legalább harminc akadémiai kutatócsoport foglalkozott a paklitaxel totálszintézisének megvalósításával, egyszerűbb természetes vegyületekből vagy más elérhető kiindulási anyagokból.[44] A totálszintézis kidolgozását a kémiai kíváncsiság motiválta, mintsem a gyakorlati alkalmazhatósága. Az első sikeres kutatócsoport, akik egy jóval egyszerűbb kiindulási anyagból állították elő a paklitaxelt, Robert A. Holtoné volt, akiknek elsőként fogadták el a cikküket, míg K. C. Nicolau publikációja jelent meg először nyomtatásban (1994. február 24.). Holton cikkének benyújtása egy hónappal megelőzte Nicolaouét (1993. december 21. vs. 1994. január 24.).[45] A közeli egybeesést kutatócsoportok többéves verejtékes munkájának fényében nagyon szoros versenynek,[46] illetve döntetlennek titulálták,[44] bár mindkét csoport vitatja, hogy melyiküké a hatékonyabb szintetikus stratégia és taktika.[46]
2006-ig öt másik kutatócsoport számolt be sikeres totálszintézisről: Wender és munkatársai 1997-ben, Kuwajima és munkatársai illetve Mukaiyama és munkatársai 1998-ban (lineáris szintézissel), míg Danishefsky és munkatársai 1996-ban, illetve Takahashi és munkatársai 2006-ban (konvergens szintézissel). Ezen szintetikus stratégiák mindegyike az ABCD gyűrűrendszerű 10‑dezacetil-baccatin típusú alapváz előállítását célozza meg, amit általában a 13-as szénatom hidroxilcsoportjára kapcsolódó farok rész kiépítése követ.[44] A farokrész egy (2R,3S)-3-benzamido-2-hidroxi-3-fenilpropánsav, aminek szelektív enzimkatalizált szintézisét Forró és munkatársai oldottak meg 2015-ben.[47]
Habár a paklitaxel totálszintézise lehetővé teszi új analógok előállítását, amely feltétele a hatás-szerkezet összefüggések feltárásának, a totálszintézis nem a kereskedelmi előállítást szolgálta.[48]
Költségek
szerkesztésAz NHS adatai alapján korai mellrákban szenvedő betegekre jutó egyéni költség, négy ciklust feltételezve 4000 angol font (kb. 6000 US$) volt 2011-ben.[49]
Történelem
szerkesztésA paklitaxel 1962-ben fedezték fel az NCI által finanszírozott szűrőprogram keretében.[7] Az amerikai tiszafa (Taxus brevifolia) kérgéből történő izolálást 1971-ben Monroe E. Wall és Mansukh C. Wani hajtották végre (Research Triangle Institute, Research Triangle Park, Észak-Karolina).[50] A Taxus név után kapta a hatóanyag a taxol elnevezést, míg a paklitaxel generikus gyógyszernevet a BMS adta.
Növényi szűrővizsgálati program
szerkesztés1955-ben az NCI megalapította a Cancer Chemotherapy National Service Centert (CCNSC), egy olyan nyilvános szűrőközpontot létrehozva, ahol külső intézetek és vállalatok által benyújtott vegyületek daganatellenes hatásának vizsgálata vált lehetségessé.[51] A vizsgált vegyületek többsége szintetikus volt, viszont 1958-tól az ott dolgozó Jonathan Hartwell vegyész korábbi tapasztalatai természetes eredetű származékokkal arra ösztönözték, hogy növényeket is bevonjanak a vizsgálatokba.[52] Néhány éves nem hivatalos megállapodás után, 1960 júliusában az NCI megbízta az Amerikai Egyesült Államok Földművelésügyi Minisztérium (United States Department of Agriculture, USDA) botanikusait évi 1000 növényi minta begyűjtésével.[53] 1962. augusztus 21-én Arthur S. Barclay botanikus egy amerikai tiszafa kérgéből vett mintát a Packwood közeli erdőben, ami egy négy hónapos gyűjtőút része volt. A mintát a CCNSC szakértői feldolgozták, s ami 1964. május 22-én egy vizsgálatban citotoxikusnak bizonyult.[54]
1964 végén illetve 1965 elején, a Monroe E. Wall vezette a frakcionálást és izolálást végző labort az észak-karolinai Research Triangle Parkban. A friss Taxus mintákból 1966. szeptemberében sikerült izolálni a hatóanyagot, majd eredményeiket 1967. áprilisában jelentették be a Miami Beach-ben tartott Amerika Kémiai Társaság (American Chemical Society, ACS) megbeszélésén.[55] 1967 júniusában kapta az aktív hatóanyag a „taxol” elnevezést.[54] 1971-ben Wall és kollégája, Wani publikálták a kémiai szerkezetet is tartalmazó eredményeiket.[56]
Az NCI folytatta a tiszafakéreg gyűjtésére irányuló munkát, hogy nagyobb mennyiségű taxolt tudjanak izolálni. 1969-re 28 kg nyers extraktumot nyertek ki hozzávetőlegesen 1200 kg kéregből, amiből mindössze 10 g tiszta hatóanyagot nyertek ki,[57] de ez néhány évig még nem került felhasználásra. 1975-ben a taxol egy másik in vitro kísérletben is mutatott biológiai aktivitást, majd két év múlva egy új intézet áttekintette a korábbi adatokat, és további tesztelésre javasolta.[58] Ez legalább 600 grammos mennyiséget jelentett tisztított taxolból, 1977-ben pedig további 3200 kg kérget.
1978-ban az NCI két kutatója a taxol enyhe pozitív eredményekről számolt be leukémiás egerek kezelésében.[59] 1978 novemberében a taxol hatásosnak bizonyult xenograftokkal végzett kísérletekben.[60] Eközben a taxol kezdett ismertté válni a sejtbiológiában és a rákkutatók között is, köszönhetően Susan B. Horwitz (az Albert Einstein College of Medicine molekuláris farmakológusa) 1979-es publikációjának, amelyben a taxol korábban ismeretlen hatásmechanizmusát, azaz a mikrotubulus-rendszer stabilizáló hatását írta le. A formulációs problémákkal együtt, a taxol iránti fokozott érdeklődés a kutatók részéről azt jelentette, hogy az NCI-nek 9100 kg tiszafa kérget kellett előirányoznia.[61] Az állatokon végzett toxicitási vizsgálatok 1982 júniusában fejeződtek be, majd novemberben az NCI benyújtotta kísérleti új gyógyszer (Investigational New Drug, IND) kérelmét az FDA-nak, amely nélkülözhetetlen a humán klinikai vizsgálatok megkezdéséhez.[61]
Korai klinikai vizsgálatok, ellátás és szállítás
szerkesztésA fázis I vizsgálat 1984 áprilisában kezdődött, a fázis II pedig egy évvel később.[62] A nagyobb volumenű vizsgálatok nagyobb hatóanyagigénnyel is jártak, így további 5400 kg tiszafakéreg begyűjtése vált szükségessé, ami lehetővé tette a fázis II vizsgálat elindítását 1986 végén. A taxol iránti igény felismerése után, még legkevesebb 27 tonna kéreg begyűjtését helyezték kilátásba. Ez a példátlan nagy mennyiségű kéreg apropóján először merült fel a tiszafa populáció veszélyeztetésének kérdése mint ökológiai probléma, amikor helyi politikusok és erdészek fejezték ki nyugtalanságukat a programmal kapcsolatban.[63]
A fázis II első nyilvános jelentése 1988 májusában volt, amelyben a taxol hatásosságát mutatták ki melanómában szenvedő betegeken, illetve rezisztens petefészekrákban szenvedők 30%-os reagálási arányáról számoltak be.[64] Ezen a ponton az NCI Natural Product Branch részlegén dolgozó Gordon Cragg kiszámolta a petefészekrák és a melanóma kezeléséhez elegendő taxol mennyiséget, és azt találta, hogy évi 360 000 fa kivágásával lehetne ezt biztosítani. Ekkor először merültek fel komolyabb átgondolások az ellátást illetően.[63] Látva a ráháruló feladat méretét, az NCI egy gyógyszergyárral való együttműködés megkötése mellett döntött. 1989 augusztusában megjelentették az amerikai kormány és a magánvállalatok közötti együttműködési tervüket (CRADA), felajánlva a jelenlegi készletet és a kéreg ellátását, valamint védett hozzáférést az eddig összegyűjtött adatokhoz, s mindezt azért, hogy hajlandó legyen elköteleződni egy vállalat, hogy nyersanyagot biztosítson, taxolt izoláljon, és támogassa nagyobb volumenű klinikai vizsgálatokat. A taxolt leíró Goodman és Welsh szavaival élve „Az NCI gondolkodik, de nem együttműködésen… hanem a taxol átruházásán (összes problémájával együtt)”.[63]
Habár az ajánlatot széles körben hirdették, csupán négy vállalat jelentkezett, köztük az amerikai Bristol-Myers Squibb (BMS), akit végül 1989 decemberében választottak ki partnernek. A BMS kiválasztásával kapcsolatban különböző híresztelések kaptak szárnyra, ezügyben 1991-ben és 1992-ben kongresszusi meghallgatások is zajlottak. Az NCI-nek kevés esélye volt megfelelő partnert találni, a megállapodás feltételei mégis ellentmondásosnak tűntek. Az USA számvevőszékének (Government Accountability Office, GAO) 2003-as jelentése szerint az NCI nem vette figyelembe a költséghatékonyságot.[65] A CRADA-val összhangban az USDA és a Belügyminisztérium kizárólagos állami ellátást biztosított a Taxus brevifoliából a BMS részére. A kritikák szerint, ezzel a kizárólagos szerződéssel a BMS bizonyos monopóliumhoz jutott.[66] Tizennyolc hónappal a CRADA után, új gyógyszer kérelmet (New Drug Application, NDA) nyújtott be, amit az FDA 1992 végén el is fogadott.[63] Habár nem állt szabadalmi védelem alatt a hatóanyag, a Waxman-Hatch-Act rendelkezései ötéves kizárólagos piaci forgalmazásra adtak jogot.
1990-ben a BMS Taxol® kereskedelmi nevet kérelmezte a taxolnak, amit 1992-ben elfogadtak. Ezzel egy időben a taxol, mint vegyület, a paklitaxel generikus nevet (INN) kapta. Kritikusok, köztük a Nature is bírálta a döntést, mivel a taxol elnevezés már több mint két évtizede használatban volt, s több mint 600 tudományos értekezés tartalmazta, ezért nem javasolták a kereskedelmi elnevezés odaítélését, és a BMS ezen jogának lemondását követelték.[67] A BMS nem akarta megváltoztatni döntését arra hivatkozva, hogy egy új név zavart keltene az onkológusok között, és veszélyeztetné a betegek biztonságát. Később bíróságon védte meg a név feletti jogát.[68] A BMS-t Goodman és Walsh idézetének elferdítésével is kritizálták.[69]
2000-ben a taxol éves forgalma 1,6 milliárd US dollár volt. A Taxol-nak immáron generikumai is megjelenhetnek, ugyanis nem védi szabadalom. 2007 októberében Indiában is elfogadták mellrákos betegek kezelésére.
Elnevezés
szerkesztésA paklitaxel elnevezésének a tetraciklikus 17 szénatomos (heptadekán) váz szolgál alapul. Összesen 11 királitáscentrumot tartalmaz. Az aktív sztereoizomer a (−)-paklitaxel, ami az ábrán látható.
(1S,2S,3R,4S,7R,9S,10S,12R,15S)-4,12-Diacetoxi-15-{[(2R,3S)-3- (benzoilamino)-2-hidroxi-3- fenilpropanoil]oxi}-1,9- dihidroxi-10,14,17,17-tetrametil -11-oxo-6-oxatetraciklo [11.3.1.0~3,10~.0~4,7~] heptadek-13-én-2-il rel-benzoát
Újabb kutatások
szerkesztésEgy 2013-as tanulmány alapján a koffein gátolja a paklitaxel által indukált apoptózist rákos vastagbélsejteken.[70] A klinikai alkalmazás mellett a paklitaxelt intenzíven használják biológiai és orvosi kísérletekben, mint mikrotubulus stabilizáló. Általánosságban, a mikrotubulusokat érintő in vitro vizsgálatokban, például motilitás vizsgálatokban, paklitaxelt alkalmaznak a mikrotubulusok integritásának fenntartásában, amennyiben hiányoznak a különböző nukleációs faktorok és más sejtben található stabilizáló elemek. Többek között használják még a mikrotubulus motorfehérjék viselkedésének módosítására szánt gyógyszerek in vitro kísérleteiben, ugyanakkor mutáns motor fehérjék tanulmányozásában is. Tesztelték in vitro inzulin aggregáció gátlására 10:1 arányban (inzulin:paklitaxel) amelyben az inzulin aggregáció közel 70%-kal csökkent. Izoterm kalorimetriás (ITC) titrálások alapján a paklitaxel hidrogénhíd kötéseken és van der Waals-féle kölcsönhatásokon keresztül kötődik az inzulinhoz.[71] A paklitaxel gátló hatását fehérje oldat kolloidális stabilizáló képességének tulajdonítják, amit paklitaxel által gátolt lizozim fibrilláció során figyeltek meg, „off-pathway" oligomer köztitermékek indukálását követően.[72] A paklitaxelt in vivo kísérletekben is használják, mint például ecetmuslicáknál (Drosophila melanogaster), vagy egyedi sejtekbe injektálják mikrotubulus stabilizálására, vagy pedig a mikrotubulusok számának növelése céljából. A paklitaxel indukálja a myelin újratermelődését egerekben,[73] és a metilészter származéka gátolja a hPAD2-t in vitro kísérletben.[74] Az Angiotech Pharmaceuticals Inc. 1999-ben klinikai II-es vizsgálatban paklitaxel alkalmazását tesztelte sclerosis multiplex kezelésében,[75] azonban 2002-es eredmények alapján nem volt szignifikáns javulás a betegek állapotában.[76]
2016-ban exoszómába csomagolt paklitaxellel kezeltek több gyógyszerrel szemben ellenálló rákos egérsejteket, melyben a hagyományos bevitt dózis tizenötöde már elég volt azonos hatás eléréséhez. Ugyanakkor jelzett exoszómákkal sikerült megjelölni tumorsejteket, amely új diagnosztikai módszerek kifejlesztéséhez vezethet.[77][78]
További képek
szerkesztés-
A paklitaxel kalottamodellje
-
A paklitaxel forgó molekulamodelle
-
A paklitaxel kristályszerkezete
-
A paklitaxel felszíni teljes töltése, konformációja energia minimumon
Készítmények
szerkesztésABRAXANE 5 mg/ml por szuszpenziós infúzióhoz
PACLITAXEL ACCORD 6 mg/ml koncentrátum oldatos infúzióhoz
PACLITAXEL-TEVA 6 mg/ml koncentrátum oldatos infúzióhoz
Hivatkozások
szerkesztés- ↑ (2006) „Enhanced Oral Paclitaxel Bioavailability After Administration of Paclitaxel-Loaded Lipid Nanocapsules”. Pharmaceutical Research 23 (6), 1243–50. o. DOI:10.1007/s11095-006-0022-2. PMID 16715372.
- ↑ a b c d Paclitaxel. The American Society of Health-System Pharmacists. [2017. szeptember 14-i dátummal az eredetiből archiválva]. (Hozzáférés: 2015. január 2.)
- ↑ (2012. július 13.) „Taxanes during Pregnancy: Probably Safe, but Still to Be Optimized”. Oncology 83 (4), 239–240. o. DOI:10.1159/000341820. PMID 22907122.
- ↑ Nirmala Chandralega Kampan, Mutsa Tatenda Madondo, Orla M. McNally, Michael Quinn, and Magdalena Plebanski (2015. July). „Paclitaxel and Its Evolving Role in the Management of Ovarian Cancer”. BioMed Research International. DOI:10.1155/2015/413076. (Hozzáférés: 2019. december 23.)
- ↑ III.5.1.2. Alkaloidok, Gyógynövény és Drogismeret Farmakognózia – Fitokémia, gyógynövények alkalmazása. Semmelweis Egyetem (2012). Hozzáférés ideje: 2019. december 23.
- ↑ Analogue-based Drug Discovery [archivált változat] (angol nyelven). John Wiley & Sons, 512. o. (2006. július 13.). ISBN 9783527607495 [archiválás ideje: 2016. december 21.]
- ↑ a b c Taxol® (NSC 125973). National Cancer Institute. [2015. szeptember 5-i dátummal az eredetiből archiválva]. (Hozzáférés: 2016. február 14.) Wayback machine
- ↑ WHO Model List of Essential Medicines (19th List). World Health Organization, 2015. április 1. [2016. december 13-i dátummal az eredetiből archiválva]. (Hozzáférés: 2016. december 8.)
- ↑ Paclitaxel. International Drug Price Indicator Guide . [2018. január 22-i dátummal az eredetiből archiválva]. (Hozzáférés: 2016. december 8.)
- ↑ British national formulary : BNF 69, 69, British Medical Association, 623. o. (2015. július 13.). ISBN 9780857111562
- ↑ (1995) „Treatment of HIV-associated Kaposi's sarcoma with paclitaxel”. The Lancet 346 (8966), 26–8. o. DOI:10.1016/S0140-6736(95)92654-2. PMID 7603142.
- ↑ a b Pharmindex ABRAXANE 5 mg/ml por szuszpenziós infúzióhoz. (Hozzáférés: 2019. június 26.)
- ↑ a b Pharmindex PACLITAXEL ACCORD 6 mg/ml koncentrátum oldatos infúzióhoz. (Hozzáférés: 2019. június 26.)
- ↑ British National Formulary. [2020. március 14-i dátummal az eredetiből archiválva]. (Hozzáférés: 2019. június 26.)
- ↑ Paclitaxel, Protein-Bound Suspension. Paclitaxel, Protein-Bound Suspension . Cancer.Org, 2015. január 6. [2020. május 12-i dátummal az eredetiből archiválva]. (Hozzáférés: 2015. január 24.)
- ↑ Product Information: TAXOL(R) IV injection, paclitaxel IV injection. Bristol-Myers Squibb Company, Princeton, NJ, 2013. Accessed from https://www.accessdata.fda.gov/drugsatfda_docs/label/2015/020262s051lbl.pdf on 4 October 2018.
- ↑ Gelderblom H (2001). „Cremophor EL”. European Journal of Cancer 37 (13), 1590–1598. o. DOI:10.1016/S0959-8049(01)00171-X. PMID 11527683.
- ↑ "Abraxane Drug Information Archiválva 2005. május 26-i dátummal a Wayback Machine-ben.." Food and Drug Administration. January 7, 2005. Retrieved on March 9, 2007.
- ↑ Product Information: ABRAXANE(R) intravenous injection suspension, paclitaxel protein-bound particles intravenous injection suspension. Celgene Corporation (per FDA), Summit, NJ, 2018. Accessed from https://www.accessdata.fda.gov/drugsatfda_docs/label/2018/021660s045lbl.pdf on 4 October 2018.
- ↑ Gyires Zsuzsa, Fürst Zsuzsanna. A farmakológia alapjai. Medicina Könyvkiadó Zrt. (2011.)
- ↑ (2008) „Taxanes from Shells and Leaves ofCorylus avellana”. Journal of Natural Products 71 (1), 58–60. o. DOI:10.1021/np0704046. PMID 18163585.
- ↑ (2001) „Paclitaxel stent coating inhibits neointimal hyperplasia at 4 weeks in a porcine model of coronary restenosis”. Circulation 103 (18), 2289–95. o. DOI:10.1161/01.CIR.103.18.2289. PMID 11342479.
- ↑ "Medline Plus Entry for Paclitaxel Injection Archiválva 2010. február 12-i dátummal a Wayback Machine-ben.." MEDLINE. Last Reviewed 09/01/2008. Accessed 10-2-21.
- ↑ (2001) „Refined structure of $alpha;$beta;-tubulin at 3.5 p resolution1”. Journal of Molecular Biology 313 (5), 1045–57. o. DOI:10.1006/jmbi.2001.5077. PMID 11700061.
- ↑ (2004) „The spindle checkpoint, aneuploidy, and cancer”. Oncogene 23 (11), 2016–27. o. DOI:10.1038/sj.onc.1207374. PMID 15021889.
- ↑ (2008) „Microtubules do not promote mitotic slippage when the spindle assembly checkpoint cannot be satisfied”. The Journal of Cell Biology 182 (4), 623–9. o. DOI:10.1083/jcb.200805072. PMID 18710927.
- ↑ (2004) „Microtubules as a target for anticancer drugs”. Nature Reviews. Cancer 4 (4), 253–65. o. DOI:10.1038/nrc1317. PMID 15057285.
- ↑ (2010) „Paclitaxel-dependent cell lines reveal a novel drug activity”. Molecular Cancer Therapeutics 9 (11), 2914–23. o. DOI:10.1158/1535-7163.MCT-10-0552. PMID 20978163.
- ↑ „Medicinal tree used in chemotherapy drug faces extinction”, The Guardian, 2011. november 10.. [2017. február 16-i dátummal az eredetiből archiválva] (Hozzáférés: 2017. február 15.)
- ↑ Goodman & Walsh 2001, 172–5. o.
- ↑ Goodman & Walsh 2001, 100–1. o.
- ↑ Paclitaxel Injection, USP (amerikai angol nyelven). Injectable Pharmaceuticals . [2016. szeptember 18-i dátummal az eredetiből archiválva]. (Hozzáférés: 2016. április 22.)
- ↑ History. [2016. május 24-i dátummal az eredetiből archiválva]. (Hozzáférés: 2016. április 22.)
- ↑ Phyton BioTech Paclitaxel. [2016. augusztus 7-i dátummal az eredetiből archiválva]. (Hozzáférés: 2016. április 22.)
- ↑ Imseng, Nicole. Suspension Culture of Plant Cells under Heterotrophic Conditions.. Wiley-Blackwell, 224–257. o. (2014). ISBN 978-3-527-33547-3
- ↑ Gilbert Gorr and Roland Franke. Commercial Pharmaceutical Production of Complex APIs via Plant Cell Fermentation (PCF®) Technology. Presentation at CPhI 2015, Oct. 13th.
- ↑ 2004 Greener Synthetic Pathways Award: Bristol-Myers Squibb Company: Development of a Green Synthesis for TAXOL Manufacture via Plant Cell Fermentation and Extraction. [2006. október 2-i dátummal az eredetiből archiválva].
- ↑ (1993) „Taxol and taxane production by Taxomyces andreanae, an endophytic fungus of Pacific yew”. Science 260 (5105), 214–6. o. DOI:10.1126/science.8097061. PMID 8097061.
- ↑ (2004) „Study on the Preparation and Regeneration of Protoplast from Taxol-producing Fungus Nodulisporium sylviforme”. Nature and Science 2 (2), 52–59. o. DOI:10.7537/marsnsj020204.09.
- ↑ (2009) „Taxomyces andreanae: A Presumed Paclitaxel Producer Demystified?”. Planta Med 75 (15), 1561–6. o. DOI:10.1055/s-0029-1186181. PMID 19809969.
- ↑ (2013) „Getting to the bottom of taxol biosynthesis by fungi”. Fungal Diversity 60, 161–170. o. DOI:10.1007/s13225-013-0228-7.
- ↑ (2011) „Simultaneous production and partitioning of heterologous polyketide and isoprenoid natural products in an Escherichia coli two-phase bioprocess”. Journal of Industrial Microbiology & Biotechnology 38 (11), 1809–1820. o. DOI:10.1007/s10295-011-0969-9. PMID 21487833.
- ↑ (2008) „Metabolic engineering of taxadiene biosynthesis in yeast as a first step towards Taxol (Paclitaxel) production”. Metabolic Engineering 10 (3–4), 201–6. o. DOI:10.1016/j.ymben.2008.03.001. PMID 18485776.
- ↑ a b c Nina Hall, 2003, Creating complexity: The beauty and logic of synthesis, Chem. Commun., 661 – 664, doi:10.1039/b212248k
- ↑ See N. Hall, ibid. See also the American Chemical Society publication Chemical and Engineering News (C&EN), Feb. 21, 1994, page 32, and primary citations appearing at Holton and Nicolaou taxol total synthesis articles.
- ↑ a b Flam, Faye (1994). „Race to synthesize Taxol ends in a tie”. Science 263 (5149), 911. o. DOI:10.1126/science.7906053. PMID 7906053.
- ↑ Forró, Enikő, Zala (2015. június 1.). „Novel chemo-enzymatic route to a key intermediate for the taxol side-chain through enantioselective O-acylation. Unexpected acyl migration” (angol nyelven). Journal of Molecular Catalysis B: Enzymatic 116, 101–105. o. DOI:10.1016/j.molcatb.2015.03.015.
- ↑ Goodman & Walsh 2001, 179–182. o.
- ↑ NICE Guidance TA108. [2007. június 30-i dátummal az eredetiből archiválva].
- ↑ (1995. február 15.) „amptothecin and taxol: discovery to clinic—thirteenth Bruce F. Cain Memorial Award Lecture.”. Cancer Res. 55 (4), 753–60. o. [2016. november 24-i dátummal az eredetiből archiválva]. PMID 7850785.
- ↑ Goodman & Walsh 2001, 17. o.
- ↑ Goodman & Walsh 2001, 22. o.
- ↑ Goodman & Walsh 2001, 25,28. o.
- ↑ a b Goodman & Walsh 2001, 51. o.
- ↑ (1995) „Camptothecin and taxol: Discovery to clinic—thirteenth Bruce F. Cain Memorial Award Lecture”. Cancer Research 55 (4), 753–60. o. PMID 7850785.
- ↑ (1971) „Plant antitumor agents. VI. The isolation and structure of taxol, a novel antileukemic and antitumor agent from Taxus brevifolia”. J Am Chem Soc 93 (9), 2325–7. o. DOI:10.1021/ja00738a045. PMID 5553076.
- ↑ Goodman & Walsh 2001, 81. o.
- ↑ Goodman & Walsh 2001, 79,81. o.
- ↑ (1978) „Cytologic evidence that taxol, an antineoplastic agent from Taxus brevifolia, acts as a mitotic spindle poison”. Cancer Treatment Reports 62 (8), 1219–22. o. PMID 688258.
- ↑ Goodman & Walsh 2001, 95. o.
- ↑ a b Goodman & Walsh 2001, p. 97
- ↑ Goodman & Walsh 2001, 115. o.
- ↑ a b c d Goodman & Walsh 2001, p. 120
- ↑ Rowinsky, EK (1988). „Phase II study of taxol in advanced epithelial malignancies”. Proceedings of the Association of Clinical Oncology 7, 136. o.
- ↑ Technology Transfer: NIH-Private Sector Partnership in the Development of Taxol. [2007. július 26-i dátummal az eredetiből archiválva]. (Hozzáférés: 2016. július 17.)
- ↑ Nader, Ralph; Love, James. "Looting the medicine chest: how Bristol-Myers Squibb made off with the public's cancer research." The Progressive. February 1993. Retrieved on March 9, 2007.
- ↑ (1995) „Names for hi-jacking”. Nature 373 (6513), 370. o. DOI:10.1038/373370a0. PMID 7830775.
- ↑ Goodman & Walsh 2001, 170. o.
- ↑ Bristol-Myers Squibb, The development of TAXOL (paclitaxel), March 1997, as cited in Goodman & Walsh 2001, p. 2
- ↑ Mhaidat, NM (2014. január 1.). „Caffeine inhibits paclitaxel‑induced apoptosis in colorectal cancer cells through the upregulation of Mcl-1 levels”. J Mol Med Rep 9 (1), 243–8. o. [2015. június 22-i dátummal az eredetiből archiválva]. DOI:10.3892/mmr.2013.1763. PMID 24173825.
- ↑ (2014) „Inhibition study on insulin fibrillation and cytotoxicity by paclitaxel”. The Journal of Biochemistry 155 (6), 361–373. o. DOI:10.1093/jb/mvu012. PMID 24535601.
- ↑ (2018) „Paclitaxel inhibited lysozyme fibrillation by increasing colloidal stability through formation of "off-pathway" oligomers”. Int J Biol Macromol 111, 870–879. o. DOI:10.1016/j.ijbiomac.2018.01.072. PMID 29352977.
- ↑ (2002) „Paclitaxel (Taxol) attenuates clinical disease in a spontaneously demyelinating transgenic mouse and induces remyelination”. Multiple Sclerosis (Houndmills, Basingstoke, England) 8 (2), 130–8. o. DOI:10.1191/1352458502ms776oa. PMID 11990870.
- ↑ (2008) „Kinetics of human peptidylarginine deiminase 2 (hPAD2)--reduction of Ca2+ dependence by phospholipids and assessment of proposed inhibition by paclitaxel side chains”. Biochemistry and Cell Biology 86 (5), 437–47. o. DOI:10.1139/o08-124. PMID 18923545.
- ↑ MS Society of Canada Phase II Clinical trial of Micellar Paclitaxel for secondary-progressive MS underway in Canada Archiválva 2012. március 15-i dátummal a Wayback Machine-ben.
- ↑ MS Society of Canada Angiotech Halts Study of Micellar Paclitaxel stating no benefit of statistical significance seen Archiválva 2012. március 15-i dátummal a Wayback Machine-ben.
- ↑ Lavars, Nick: Cloaking chemo drugs in cellular bubbles destroys cancer with one fiftieth of a regular dose. www.gizmag.com , 2016. január 14. [2016. február 24-i dátummal az eredetiből archiválva]. (Hozzáférés: 2016. február 14.)
- ↑ Kim, Myung Soo (2016). „Development of exosome-encapsulated paclitaxel to overcome MDR in cancer cells”. Nanomedicine: Nanotechnology, Biology and Medicine 12 (3), 655–664. o. DOI:10.1016/j.nano.2015.10.012. PMID 26586551.
Fordítás
szerkesztésEz a szócikk részben vagy egészben a Paclitaxel című angol Wikipédia-szócikk ezen változatának fordításán alapul. Az eredeti cikk szerkesztőit annak laptörténete sorolja fel. Ez a jelzés csupán a megfogalmazás eredetét és a szerzői jogokat jelzi, nem szolgál a cikkben szereplő információk forrásmegjelöléseként.