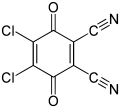
5,6-Diciano-2,3-diklór-1,4-benzokinon
| 5,6-Diciano-2,3-diklór-1,4-benzokinon[1] | |||
| |||
| Más nevek | 5,6-diciano-2,3-diklór-p-benzokinon 4,5-diklór-3,6-dioxo-1,4-ciklohexadién-1,2-dikarbonitril diklór-diciano-benzokinon | ||
| Kémiai azonosítók | |||
|---|---|---|---|
| Rövidítés | DDQ | ||
| CAS-szám | 84-58-2 | ||
| PubChem | 6775 | ||
| ChemSpider | 6517 | ||
| EINECS-szám | 201-542-2 | ||
| RTECS szám | GU4825000 | ||
| |||
| |||
| InChIKey | HZNVUJQVZSTENZ-UHFFFAOYSA-N | ||
| Kémiai és fizikai tulajdonságok | |||
| Kémiai képlet | C8Cl2N2O2 | ||
| Moláris tömeg | 227,00 g/mol | ||
| Megjelenés | sárga-narancssárga por | ||
| Sűrűség | 1,7 g/cm³ | ||
| Olvadáspont | 210–215 °C (bomlik) | ||
| Forráspont | 301,8°C (760 Hgmm nyomáson) | ||
| Oldhatóság (vízben) | reagál | ||
| Veszélyek | |||
| R mondatok | R25 R29 | ||
| S mondatok | S22 S24/25 S37 S45 | ||
| Lobbanáspont | 136,3°C | ||
| Ha másként nem jelöljük, az adatok az anyag standardállapotára (100 kPa) és 25 °C-os hőmérsékletre vonatkoznak. | |||
Az 5,6-diciano-2,3-diklór-1,4-benzokinon (vagy DDQ) szerves vegyület, összegképlete C8Cl2N2O2. Oxidáló tulajdonsága folytán a szerves kémiai reakciók hasznos reagense alkoholok,[2] fenolok[3] és szteroid ketonok[4] dehidrogénezési reakcióiban. Vízben bomlik, de ásványi savak vizes oldatában stabil.
Előállítása
szerkesztésElőállítása 1,4-benzokinon ciánozásával és klórozásával történik. Thiele és Günther először egy 6 lépéses előállítási módot írt le 1906-ban.[5] A vegyület nem váltott ki érdeklődést, míg fel nem fedezték, hogy dehidrogénezőszerként használható. Egylépéses, 2,3-dicianohidrokinon klórozásával történő előállításáról 1965-ben számoltak be.[6]
Stabilitása
szerkesztésVízzel reagál, melynek során rendkívül mérgező hidrogén-cianid (HCN) keletkezik. Száraz helyen tárolandó, az alacsony hőmérséklet és enyhén savas környezet növelheti stabilitását.
Felhasználása
szerkesztésA szerves kémiában reagensként használják, enyhe oxidálószer és gyökfogó.
Reakciói
szerkesztés1. dehidrogénezés
szerkesztés2. aromatizáció
szerkesztés3. oxidatív kapcsolás
szerkesztésFordítás
szerkesztésEz a szócikk részben vagy egészben a(z) 2,3-Dichloro-5,6-dicyano-1,4-benzoquinone című angol Wikipédia-szócikk ezen változatának fordításán alapul. Az eredeti cikk szerkesztőit annak laptörténete sorolja fel. Ez a jelzés csupán a megfogalmazás eredetét és a szerzői jogokat jelzi, nem szolgál a cikkben szereplő információk forrásmegjelöléseként.
Hivatkozások
szerkesztés- ↑ 2,3-Dichloro-5,6-dicyano-p-benzoquinone Archiválva 2022. február 15-i dátummal a Wayback Machine-ben at Sigma-Aldrich
- ↑ Braude, E. A; Linstead, R. P.; Wooldridge, K. R. H. (1956). „593. Hydrogen Transfer. Part IX The Selective Dehydrogenation of Unsaturated Alcohols by High-potential Quinones”. Journal of the Chemical Society (Resumed) 1956, 3070–3074. o. DOI:10.1039/JR9560003070.
- ↑ Becker, H. D. (1965). „Quinone Dehydrogenation. I. Oxidation of Monohydric Phenols”. Journal of Organic Chemistry 30 (4), 982–989. o. DOI:10.1021/jo01015a006.
- ↑ Turner, A. B.; Ringold, H. J. (1967). „Applications of High-potential Quinones. Part I. The Mechanism of Dehydrogenation of Steroidal Ketones by 2,3-Dichloro-5,6-Dicyanobenzoquinone”. Journal of the Chemical Society C: Organic 1967, 1720–1730. o. DOI:10.1039/J39670001720.
- ↑ Thiele, J.; Günther, F. (1906). „Ueber Abkömmlinge des Dicyanhydrochinons”. Justus Liebig's Annalen der Chemie 349 (1), 45–66. o. DOI:10.1002/jlac.19063490103.
- ↑ Walker, D.; Waugh, T. D. (1965). „2,3-Dichloro-5,6-Dicyanobenzoquinone (DDQ). A New Preparation”. The Journal of Organic Chemistry 30 (9), 3240–3240. o. DOI:10.1021/jo01020a529.
- ↑ Brown, W.; Turner, A. B. (1971). „Application of High-potential Quinones. 7. Synthesis of Steroidal Phenanthrenes by Double Methyl Migration”. Journal of the Chemical Society C: Organic 1971, 2566–2572. o. DOI:10.1039/J39710002566.
- ↑ Zhang, Y.; Li, C. J. (2006). „DDQ-Mediated Direct Cross-Dehydrogenative-Coupling (CDC) between Benzyl Ethers and Simple Ketones”. Journal of the American Chemical Society 128 (13), 4242–4243. o. DOI:10.1021/ja060050p.