Diazometán
A diazometán a legegyszerűbb diazovegyület, képlete CH2N2. Szobahőmérsékleten, tiszta állapotban nagyon reakcióképes, mérgező sárga gáz. Nagy reakciókészsége miatt legtöbbször éteres oldatában használják fel. A diazometán ideális metilezőszer, készségesen reagál a mozgékony protont tartalmazó vegyületekkel, például karbonsavakkal vagy fenolokkal.
| Diazometán | |||
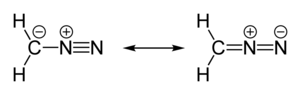 diazometán | |||
| |||
| IUPAC-név | diazometán | ||
| Kémiai azonosítók | |||
| CAS-szám | 334-88-3 | ||
| PubChem | 9550 | ||
| ChemSpider | 9176 | ||
| KEGG | C19387 | ||
| ChEBI | 73716 | ||
| |||
| |||
| InChIKey | YXHKONLOYHBTNS-UHFFFAOYSA-N | ||
| Kémiai és fizikai tulajdonságok | |||
| Kémiai képlet | CH2N2 | ||
| Moláris tömeg | 42,04 g/mol | ||
| Megjelenés | sárga színű gáz | ||
| Szag | dohos | ||
| Sűrűség | 1,4 (levegő=1) | ||
| Olvadáspont | −145 °C | ||
| Forráspont | −23 °C | ||
| Oldhatóság (vízben) | hidrolizál[1] | ||
| Kristályszerkezet | |||
| Molekulaforma | lineáris C=N=N | ||
| Dipólusmomentum | poláris | ||
| Veszélyek | |||
| Főbb veszélyek | mérgező és robbanékony | ||
| NFPA 704 | |||
| R mondatok | R12 R19 R22 R66 R67 | ||
| S mondatok | S9 S16 S29 S33 | ||
| PEL | TWA 0,2 ppm (0.4 mg/m³) | ||
| Az infoboxban SI-mértékegységek szerepelnek. Ahol lehetséges, az adatok standardállapotra (100 kPa) és 25 °C-os hőmérsékletre vonatkoznak. Az ezektől való eltérést egyértelműen jelezzük. | |||
Előállítás
szerkesztésA diazometánt többnyire N-metil-N-nitrozokarbamidból állítják elő lúggal.
Felhasználás
szerkesztésBiztonsági okokból a diazometánt mindig éteres oldatában használják fel, és közvetlenül a felhasználás előtt állítják elő. Karbonsavakból diazometánnal metil-észterek készíthetők gondot okozó melléktermék képződése nélkül, mert a keletkező nitrogéngáz elszáll, így nem szennyezi a terméket. Az átalakulás úgy értelmezhető, hogy a diazometán szénatomja protonálódik, így diazóniumion képződik. Minthogy a nem aromás diazóniumionok rendkívül bomlékonyak, azonnali nitrogénvesztés történik és metilkation keletkezik. Ez a karbonsavanionhoz kapcsolódva adja az észtert. A diazometán aldehidekkel is reagál a megfelelő keton és nitrogénmolekula képződése mellett (Buchner–Curtius–Schlotterbeck-reakció).[2][3]
Alkohollal vagy fenollal bór-trifluorid jelenlétében való reakciójakor metil-éterek állíthatók elő.
Jegyzetek
szerkesztés- ↑ ICSC 1256 - DIAZOMETHANE
- ↑ Buchner, E. (1885). „Synthese von Ketonsäureäthern aus Aldehyden und Diazoessigäther”. Berichte der Deutschen Chemischen Gesellschaft 18, 2371–2377. o. DOI:10.1002/cber.188501802118.
- ↑ Schlotterbeck, F. (1907). „The conversion of aldehydes and ketones through diazomethane”. Berichte der Deutschen Chemischen Gesellschaft 40, 479–483. o. DOI:10.1002/cber.19070400179.
Források
szerkesztés- Furka Árpád: Szerves kémia, Tankönyvkiadó, Budapest., 1988. ISBN 963 18 1258 8
