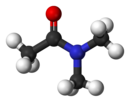
Dimetilacetamid
| Dimetilacetamid | |||
 |
| ||
| IUPAC-név | N,N-dimetilacetamid | ||
| Más nevek | DMAc, DMA, ecetsav-dimetilamid, dimetilacetamid, acetildimetilamin | ||
| Kémiai azonosítók | |||
|---|---|---|---|
| CAS-szám | 127-19-5 | ||
| PubChem | 31374 | ||
| ChemSpider | 29107 | ||
| RTECS szám | AB7700000 | ||
| |||
| |||
| InChIKey | FXHOOIRPVKKKFG-UHFFFAOYSA-N | ||
| UNII | JCV5VDB3HY | ||
| ChEMBL | 11873 | ||
| Kémiai és fizikai tulajdonságok | |||
| Kémiai képlet | C4H9NO | ||
| Moláris tömeg | 87,12 g/mol | ||
| Megjelenés | színtelen, enyhén ammóniaszagú folyadék | ||
| Sűrűség | 0,94 g/cm³ | ||
| Olvadáspont | −20 °C | ||
| Forráspont | 164–166 °C | ||
| Törésmutató (nD) | 1,4375 | ||
| Viszkozitás | 1,956 cP 25 °C-on 1,279 cP 50 °C-on | ||
| Veszélyek | |||
| Főbb veszélyek | Mérgező (T) | ||
| NFPA 704 | |||
| R mondatok | R61 R20/21 | ||
| S mondatok | S53 S45 | ||
| Lobbanáspont | 63 °C | ||
| Öngyulladási hőmérséklet | 490 °C | ||
| Rokon vegyületek | |||
| Rokon Vegyületek | Ecetsav Dimetilamin Dimetilformamid | ||
| Ha másként nem jelöljük, az adatok az anyag standardállapotára (100 kPa) és 25 °C-os hőmérsékletre vonatkoznak. | |||
A dimetilacetamid szerves vegyület képlete CH3C(O)N(CH3)2. Színtelen, vízzel elegyedő magas forráspontú folyadék, melyet a szerves kémiában gyakran használnak poláris oldószerként. A dimetilacetamid a legtöbb oldószerrel elegyedik, de alifás szénhidrogénekben rosszul oldódik.
Reakciói jellemzőek az N,N-diszubsztituált amidokra. Sav jelenlétében hidrolizál:
- CH3CON(CH3)2 + H2O + HCl → CH3COOH + (CH3)2NH2+Cl-
A dimetilacetamid jól használható erős bázisokat, például nátrium-hidroxidot használó szerves kémiai átalakítások reakcióközegeként.[1] A dimetilacetamid gyakran használt oldószer a műszálkészítésben vagy ragasztók előállításában. Gyógyszerek és lágyítószerek előállításában is használják mint reakcióközeget.
Fordítás
szerkesztésEz a szócikk részben vagy egészben a Dimethylacetamide című angol Wikipédia-szócikk ezen változatának fordításán alapul. Az eredeti cikk szerkesztőit annak laptörténete sorolja fel. Ez a jelzés csupán a megfogalmazás eredetét és a szerzői jogokat jelzi, nem szolgál a cikkben szereplő információk forrásmegjelöléseként.
Hivatkozások
szerkesztés- ↑ S. Zen and E. Kaji (1988). „Dimethyl nitrosuccinate”. Org. Synth.. ; Coll. Vol. 6: 503
