Nátrium-hidroxid
A nátrium-hidroxid (kémiai képlete: NaOH; egyéb nevei: lúgkő, marónátron, nátronlúg, marószóda,[2] zsírszóda, marólúg) szervetlen vegyületek csoportjába tartozó fémes bázis. Vízben oldva erősen lúgos oldatot képez. A 18. század előtt ez volt a legelterjedtebb lúg. Először 1736-ban egy francia tudós, Henri Louis Duhamel du Monceau nevezte nátrium-hidroxidnak. A vegyiparban erős bázikus tulajdonsága miatt széleskörűen felhasználják, főleg a textil- és papíriparban, a szappanok és mosószerek gyártásában. 1998-ban a világtermelés kb. 45 millió tonna volt. A nátrium-hidroxidot gyakran használják vegyi laboratóriumokban és a száraztisztításban. A VIII. Magyar Gyógyszerkönyvben Natrii hydroxidum néven hivatalos.
| Nátrium-hidroxid | |
 2 dimenziós szerkezet |
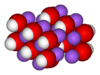 3 dimenziós szerkezet |
| IUPAC-név | nátrium-hidroxid |
| Más nevek | marószóda, nátronlúg, lúgkő, marónátron |
| Kémiai azonosítók | |
| CAS-szám | 1310-73-2 |
| PubChem | 14798 |
| ChemSpider | 14114 |
| EINECS-szám | 215-185-5 |
| RTECS szám | WB4900000 |
| Kémiai és fizikai tulajdonságok | |
| Kémiai képlet | NaOH |
| Moláris tömeg | 39,9971 g/mol |
| Megjelenés | szilárd, higroszkópos rögök |
| Halmazállapot | szilárd |
| Sűrűség | 2,1 g/cm³ |
| Olvadáspont | 318 °C |
| Forráspont | 1390 °C |
| Oldhatóság (vízben) | 111 g/100 ml (20°C) |
| Termokémia | |
| Std. képződési entalpia ΔfH |
−425,93 kJ/mol[1] |
| Veszélyek | |
| EU osztályozás | maró (C), |
| NFPA 704 | |
| R mondatok | R35 |
| S mondatok | (S1/2), S26, S37/39, S45 |
| Lobbanáspont | nem gyúlékony |
| Rokon vegyületek | |
| Azonos kation | a nátrium vegyületei |
| Azonos anion | hidroxidok |
| Az infoboxban SI-mértékegységek szerepelnek. Ahol lehetséges, az adatok standardállapotra (100 kPa) és 25 °C-os hőmérsékletre vonatkoznak. Az ezektől való eltérést egyértelműen jelezzük. | |
A tiszta nátrium-hidroxid számos formában kapható, például granulátum, pellet, vagy oldott formában. A levegőben található nedvességen kívül a szén-dioxidot is elnyeli, ezért légmentes tartályokban kell tárolni. Vízben rendkívül oldékony, valamint a folyamat erősen exoterm. Etanolban és metanolban is oldható, bár ezekben kevésbé oldódik, mint rokon vegyülete, a kálium-hidroxid. Apoláris oldószerekben (például benzolban) nem oldható. A nátrium-hidroxid sárga bevonatot hagy a fa- és papírfelületeken.
Fizikai tulajdonságok szerkesztés
- Oldáshő, ΔsolH° vizes, telített oldatban −44,45 kJ / mol; (szilárd anyag oldása vízben)
- Vizes oldatából 12,3–61,8 °C, monohidrát kristályok formájában kiválik. A kristályok olvadáspontja 65,1 °C, sűrűségük 1,829 g/cm³
- Képződéshő, Δf H° −734,96 kJ/mol;
- monohidrát −28 és −24 °C között
- heptahidrát −24 és −17,7 °C között
- pentahidrát −17,7 és −5,4 °C között
- tetrahidrát −5,4 és −12,3 °C között
- Cp moláris hőkapacitás, folyadék: 87 J/mol K, szilárd: 59 J/mol K
Kémiai tulajdonságok szerkesztés
A nátrium-hidroxid ionos vegyület, vagyis kizárólag hidroxidionokból (OH−), és nátriumionokból (Na+) áll. A nátrium-hidroxid egy nagyon erős bázis, mely savakkal könnyen sót alkot, például a hidrogén-kloriddal reagálva nátrium-klorid (konyhasó), és víz keletkezik.
Általában ezek a semlegesítés típusú reakciók egyszerűbben is felírhatók, amikor csak a hidroxid- és az oxónium-ionokkal foglalkozunk.
Ez a fajta reakció erősen exoterm. Ezen reakció segítségével az egyes savak koncentrációját is meg lehet határozni.
A nátrium-hidroxidot más, oxidok alkotta savak semlegesítésére is lehet alkalmazni. Ezek például a szén-dioxid (CO2), vagy a kén-dioxid (SO2). Általában az ipari termelés melléktermékeként felszabaduló káros gázokat lehet az ilyen reakciókkal semlegesíteni, meggátolva ezzel kikerülésüket a légkörbe.
A nátrium-hidroxid az üveggel lassan reakcióba lép, ezért a nátrium-hidroxiddal kapcsolatba kerülő üvegfelületeken nátrium-szilikát bevonat képződik.
A nátrium-hidroxid a fémek közül a vassal, és a rézzel nem lép reakcióba, viszont az alumíniummal (nátrium-[tetrahidroxo-aluminát(III)] komplex ion keletkezik), a cinkkel (nátrium-[tetrahidroxo-cinkát(II)] komplex keletkezik) viszonylag hevesen reagál. Ezért alumíniumból készült főzőedények, vagy serpenyők tisztítására nem használható. A titánt megvédi a felületén keletkező titán(III)- és titán(IV)-oxid réteg, passziválódik.
Ón(II)-klorid-oldathoz öntve a nátrium-hidroxid fehér csapadék (Sn(OH)2) képződése közben reagál. A levált ón(II)-hidroxid-csapadék lúgfeleslegben feloldódik.
Számos nemfémes elem is reakcióba léphet vele, például foszforral nátrium-hipofoszfitot alkot, szilíciummal pedig nátrium-szilikátot.
Ellentétben a nátrium-hidroxiddal, a legtöbb fém-hidroxid vízben nem oldékony, ezért az NaOH-t különféle fém-hidroxidok kicsapatására is alkalmazzák. Ilyen vegyület például az alumínium-hidroxid, melyet a vízben lévő lebegő részecskék eltávolítására alkalmaznak. Az alumínium-hidroxidot alumínium-szulfát és nátrium-hidroxid segítségével állítják elő.
A nátrium-hidroxid a különféle karbonsavakkal is heves reakcióba lép. Elég erős bázis ahhoz is, hogy a fenollal sót alkosson. A nátrium-hidroxidot az észterek, amidok, és alkil-halidok bázisvezérelt hidrolíziséhez is alkalmazzák. Ennek ellenére általában kálium-hidroxiddal helyettesítik, ugyanis az szerves oldószerekben jobban oldódik.
Ha a hideg, viszonylag híg NaOH oldatba klórgázt vezetnek, nátrium-hipoklorit (a háztartásban jól ismert hipó) keletkezik:
- 2 NaOH + Cl2 = NaOCl + NaCl + H2O
De több reakció is végbemegy:
- a klór reagál a vízzel is:
- Cl2 + H2O = HOCl+HCl
- a keletkezett HOCl (hipoklórossav) reagál a NaOH-dal, és NaOCl keletkezik.
- a keletkezett HCl reagál a NaOH-dal, és NaCl keletkezik.
Előállítása szerkesztés
1998-ban a világon 45 millió tonna nátrium-hidroxidot állítottak elő. Ebből Észak-Amerika és Ázsia körülbelül 14-14 millió tonnát, míg Európa 10 millió tonnával járult hozzá a szükségletek kielégítéséhez.
Előállításának menete szerkesztés
A nátrium-hidroxidot általában a klórral, és a hidrogénnel együtt szokták előállítani. A folyamat vízben oldott nátrium-klorid elektrolízise során megy végbe. Itt a katódnál nátrium-hidroxid válik ki, miközben hidrogéngáz szabadul fel:
- 2Na+ + 2H2O + 2e− → H2 + 2NaOH
A teljes reakció:
- 2NaCl + 2H2O → Cl2 + H2 + 2NaOH
Felhasználása szerkesztés
- A nátrium-hidroxid a vegyipar elsődleges erős bázisa. Általában vizes oldatában alkalmazzák, mert így előállítása, és szállítása is egyszerűbb, és olcsóbb. Elsősorban savak semlegesítésére alkalmazzák.
- A nátrium-hidroxidot a Bayer-eljárás során bauxitból történő alumínium-oxid előállítására is alkalmazzák.
- Savak töménységének megállapítására nagyon jól használható.
- Régebben szappan előállításra széles körben alkalmazták. A szappankészítést először az arabok alkalmazták a 7. század környékén. A cselédek tipikusan NaOH fogyasztásával követtek el öngyilkosságot, ezért forgalmazását korlátozták.
- A papírgyártás során (a nátrium-szulfiddal együtt) a cellulózrostokban található lignin elkülönítésére alkalmazzák.
- Az élelmiszeriparban széles körben alkalmazzák, például a gyümölcsök héjának kémiai úton történő eltávolítására, csokoládé és kakaó készítése során, karamellel történő színezésnél, olajbogyó tartósításánál, valamint egyes pékárukban is előfordulhat. Élelmiszer-adalékanyagként, E524 néven alkalmazzák. Napi maximum beviteli mennyisége nincs meghatározva, valamint élelmiszerek esetén nincs ismert mellékhatása, mert rendkívül erős lúgossága miatt csak nagyon kis mennyiségben alkalmazható.[3] Gyakran nátrium-karbonáttal helyettesítik.[4]
- Az állati és növényi szöveteket egyaránt nagy mértékben roncsolja.
- Néhány tudatmódosító szer (például metamfetamin) készítésénél, a gyártás során felhasznált savak semlegesítésére, vagy katalizátor nátrium előállítására alkalmazzák.[5]
Biztonsági kockázatok szerkesztés
A szilárd, vagy tömény oldatban lévő nátrium-hidroxid égési sérüléseket, maradandó sebeket, hegeket, valamint vakságot okozhat. Vízben történő oldása erősen exoterm folyamat, a felszabaduló hő égési sérülést, vagy gyúlékony anyagok belobbanását eredményezheti. Alumíniummal reagálva nagy mennyiségű hidrogén szabadul fel gáz formájában. Ezért a nátrium-hidroxidot zárt alumíniumtartályban, vagy zárt tartályban alumíniummal együtt tárolni igen veszélyes.
Jegyzetek szerkesztés
- ↑ NIST Chemistry Webbook. [2009. március 7-i dátummal az eredetiből archiválva]. (Hozzáférés: 2010. december 29.)
- ↑ http://mek.oszk.hu/00000/00060/html/073/pc007389.html
- ↑ Food-Info.net : E-numbers : E524 : Sodium hydroxide
- ↑ Hominy without Lye. National Center for Home Food Preservation
- ↑ Technical Support Document: Toxicology Clandestine Drug Labs: Methamphetamine[halott link]
Források szerkesztés
- International Chemical Safety Card 0360
- NIOSH Pocket Guide to Chemical Hazards
- European Chemicals Bureau
- Chlorine Online - Facts about Chlorine, Sodium Hydroxide (Caustic Soda) is an important co-product of Chlorine
- The Chlorine Institute, Inc. website Archiválva 2012. augusztus 27-i dátummal a Wayback Machine-ben
- Sodium hydroxide products of Bayer MaterialScience in North America
- Titration of acids with sodium hydroxide – freeware for data analysis, simulation of curves and pH calculation
- Dow Chemical Company az 50%-os oldat tulajdonságai
- N. N. Greenwood, A. Earnshaw, Chemistry of the Elements, 2nd ed., Butterworth-Heinemann, Oxford, UK, 1997.
- Heaton, A. (1996) An Introduction to Industrial Chemistry, 3rd edition, New York:Blackie. ISBN 0-7514-0272-9.
- Kirk-Othmer Encyclopedia of Chemical Technology 5th edition (online[halott link], account needed), John Wiley & Sons. Accessed November 21, 2005.
- Euro Chlor - How is chlorine made? Chlorine Online
- NIST Webbook A vízmentes nátrium-klorid adatai
