SN2 reakció
Az SN2 reakció a szerves kémiában gyakori reakciómechanizmus, melynek során egy kötés felhasadásával egy időben, azaz egy lépésben egy új kötés alakul ki. Az SN2 a nukleofil szubsztitúciós reakciómechanizmus egyik fajtája. Mivel két reagáló részecske vesz részt a lassú (sebességmeghatározó) lépésben, innen az elnevezés: (bi-molekuláris) nukleofil szubsztitúció, vagy SN2. A másik fő típus az SN1.[1]
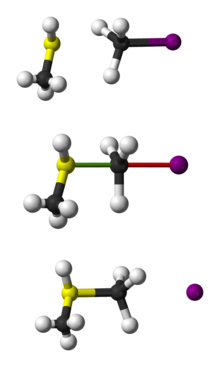

Ez a fajta reakció annyira gyakori, hogy több más elnevezése is létezik, például „bimolekuláris nukleofil szubsztitúció”, vagy szervetlen kémikusok között „asszociatív szubsztitúció” vagy „köztes csere mechanizmus”.
Reakciómechanizmus szerkesztés
A reakció leggyakrabban alifás sp3 széncentrumon játszódik le, melyhez elektronegatív, stabil távozó csoport – jellemzően halogénatom – kapcsolódik (ennek jelölése rendszerint X). A C−X kötés felhasadása és az új (gyakori jelöléssel C−T vagy C−Nu) kötés kialakulása egyidejűleg, egy átmeneti állapoton keresztül megy végbe, amelyben a nukleofilen támadott szénatom ötös koordinációjú, közelítőleg sp2 hibridizációval. A nukleofil a szénatomot a távozó csoporttal átellenes oldalon (180°-os szögben) támadja, mivel ez biztosítja a legnagyobb átfedést a nukleofil nemkötő elektronpárja és a C−X σ* lazítópálya között. A távozó csoport ezután a másik oldalon eltávolodik, így a képződő termékben a központi atom körüli tetraéderes geometria a kiindulási állapot inverze lesz.
Ha a reakció szubsztrátja királis, akkor ez gyakran inverz konfigurációt eredményez (sztereokémia), ezt Walden-inverziónak nevezzük.
Egy példa az SN2 reakcióra: a Br− (nukleofil) támadása etil-kloridon (elektrofil), ennek terméke etil-bromid, és távozó csoportként egy kloridion lép ki:
SN2 támadás akkor fordul elő, ha a szubsztráton a távozó csoporttal átellenes oldalon a szubsztituensek nem jelentenek sztérikus gátat. Emiatt ez a mechanizmus általában sztérikusan nem gátolt primer és szekunder szénatomokon játszódik le. Sztérikusan zsúfolt reakciócentrum esetén – például tercier szénatomon – a reakció SN2 helyett inkább SN1 mechanizmus szerint fog lejátszódni (az SN1 ebben az esetben azért is valószínűbb, mert kellően stabil karbokation köztitermék alakulhat ki).
A reakció sebességét befolyásoló tényezők szerkesztés
A reakció sebességét négy tényező befolyásolja:[2]
A szubsztrát szerkesztés
A szubsztrát játssza a legfontosabb szerepet a reakció sebességének meghatározásában. Ennek oka, hogy a nukleofil a szubsztrátot hátulról támadja, és ennek folyományaként hasad fel a szén és a távozó csoport közötti kötés, és alakul ki a szén–nukleofil kötés. Ezért ahhoz, hogy az SN2 reakció sebessége a lehető legnagyobb lehessen, a szubsztrátnak sztérikusan a lehető legkevésbé gátoltnak kell lennie. Összességében ez azt jelenti, hogy a metil és primer szubsztrátok reagálnak a leggyorsabban, majd ezt követik a szekunder szubsztrátok. Sztérikus gátlás miatt a tercier szubsztrátok nem vesznek részt SN2 reakcióban. Azon szerkezetek, melyek egy távozó csoport egyszerű kilépésével rendkívül stabil kationt – például rezonancia-stabilizált karbokationt – tudnak képezni, különösen hajlamosak az SN2-vel versengő SN1 úton reagálni.
Nukleofil szerkesztés
A szubsztráthoz hasonlóan a nukleofil erősségét is befolyásolja a sztérikus gátlás. A metoxid anion például erős bázis és erős nukleofil, mert metil nukleofil és így sztérikusan nincs gátolva. A terc-butoxid ezzel szemben erős bázis, de gyenge nukleofil, mert a három metilcsoport akadályozza a széncentrum megközelítését. A nukleofil erősségét a töltés és az elektronegativitás is befolyásolja: a nukleofilicitás növekszik a negatív töltés növekedésével és az elektronegativitás csökkenésével. Például a OH− jobb nukleofil, mint a víz, a I− jobb nukleofil, mint a Br− (poláris protikus oldószerben). Poláris aprotikus oldószerben a nukleofilicitás a periódusos rendszer egy oszlopán belül felfelé haladva nő, mivel az oldószer és a nukleofil között nincs hidrogénkötés; ebben az esetben a nukleofilicitás a bázicitást tükrözi. A I− így a Br−-nál gyengébb nukleofil lenne, mivel gyengébb bázis.
Oldószer szerkesztés
Az oldószer befolyásolja a reakció sebességét, mert attól függően, hogy molekulái körbeveszik-e (szolvatálják-e) a nukleofilt vagy sem, gátolhatja annak a szénatomhoz való közeledését. A poláris aprotikus oldószerek, mint a tetrahidrofurán, jobb oldószerei ennek a reakciótípusnak, mint a protikus oldószerek, mivel utóbbiak hidrogénkötést alakítanak ki a nukleofillel, ami megnehezíti a reakciócentrum támadását. A kis dielektromos állandóval rendelkező poláris protikus oldószerek vagy a gátolt végű dipólus az SN2 mechanizmusnak kedvez. Példák: DMSO, DMF, aceton stb. Poláris aprotikus oldószerben a nukleofilicitási sorrend megegyezik a bázicitási sorrenddel.
Távozó csoport szerkesztés
A távozó csoport és a szénatom közötti kötés erőssége, valamint a távozó csoport anionjának stabilitása egyaránt befolyásolja a reakció sebességét. Minél stabilabb a távozó csoport konjugált bázisa, annál nagyobb a valószínűsége, hogy a reakció során magával viszi a kötést létesítő elektronpárt. Ezért minél gyengébb konjugált bázis a távozó csoport, azaz minél erősebb sav a konjugált savja, annál könnyebben távozó csoportról van szó. Jó távozó csoportok például a halogenidek (kivéve a fluoridot, a szénatommal alkotott erős kötése miatt) és a tozilát, ezzel szemben például a HO− és H2N− nem jó távozó csoportok.
Reakciókinetika szerkesztés
Az SN2 reakció másodrendű, mivel a sebességmeghatározó lépés mind a nukleofil [Nu−], mind a szubsztrát [RX] koncentrációjától függ:
- r = k[RX][Nu−]
Ez alapvető különbség az SN1 és SN2 mechanizmusok között. Az SN1 reakció során a nukleofil a sebességmeghatározó lépés befejeződése után támad, míg az SN2 reakcióban a nukleofil a sebességmeghatározó lépésben szorítja ki a távozó csoportot. Más szóval, az SN1 reakciók sebessége csak a szubsztrát koncentrációjától függ, míg az SN2 reakció sebességét mind a szubsztrát, mind a nukleofil koncentrációja befolyásolja.
Kimutatták,[3] hogy ritka (de előre jelezhető) eseteket kivéve a primer és szekunder szubsztrátok az SN2 mechanizmus szerint reagálnak, míg a tercier szubsztrátoknál SN1 folyamat játszódik le. Két olyan tényező van, amely megnehezíti a szekunder szénatomokon lejátszódó nukleofil szubsztitúciós reakciók mechanizmusának meghatározását:
1) A vizsgált reakciók jelentős része szolvolízis, amelyben az oldószermolekula – ez gyakorta valamilyen alkohol – a nukleofil. Bár a mechanizmus másodrendű, kinetikailag a reakció elsőrendű, mivel a nukleofil – az oldószer – koncentrációja gyakorlatilag nem változik meg a reakció során. Ezt a fajta reakciót pszeudo-elsőrendű reakciónak is nevezik.
2) Azon reakciók esetében, ahol a távozó csoport maga is jó nukleofil – például bromidion –, ott a távozó csoport is indíthat SN2 reakciót (egy másik) szubsztrát molekulán. Ha a szubsztrát királis, ez inverziót okozhat még a szolvolízis előtt, racém terméket eredményezve – ami SN1 mechanizmus alapján lenne várható. Bromid távozó csoport és alkoholos oldószer esetében Cowdrey és munkatársai[4] kimutatták, hogy a bromid SN2 sebességi állandója az etanolénak 100-250-szerese.
A szekunder szubsztrátok SN1 mechanizmus szerint lejátszódó reakciónak tankönyvi példáiban mindig bromid (vagy más erős nukleofil) távozó csoport található, ami a szekunder szénatomon végbemenő alkil nukleofil szubsztitúciós reakciók megértését 80 évig akadályozta.[3] A 2-adamantil rendszeren (itt SN2 reakció nem lehetséges) Schleyer és munkatársai által,[5] valamint a Weiner és Sneen által használt (kiváló nukleofil, de nagyon rossz távozó csoport) aziddal[6][7] végzett munkák, továbbá a szulfonát távozó csoportok (nem nukleofil jó távozó csoportok) kifejlesztése, valamint Hughes és munkatársainak[3][8] munkája – mellyel kimutatták, hogy jelentős kísérleti problémák vannak az optikailag aktív 2-brómoktán eredeti SN1 mechanizmust állító szolvolitikus reakciójában – meggyőzően bizonyítják, hogy a szekunder szubsztrátok (szokatlan, de előre jelezhető esetek kivételével) kizárólag SN2 mechanizmus szerint reagálnak.
Versengő E2 reakció szerkesztés
Az SN2 reakciók során gyakori mellékreakció az E2 elimináció: az érkező anion nukleofil helyett bázisként viselkedhet, és egy proton leszakításával alként hoz létre. Ez a reakcióút akkor gyakoribb, ha az érkező ion sztérikusan gátolt, mivel ilyenkor a proton leszakítása könnyebb. Az eliminációs reakcióknak – az entrópia növekedése miatt – általában kedvez a hőmérséklet emelése.[9] Ez a hatás bemutatható szulfonát és egyszerű alkil-bromid tömegspektrométer belsejében lejátszódó reakciójával:[10][11]
Etil-bromid esetén a reakció fő terméke a szubsztitúciós termék. Ahogy az elektrofil centrum sztérikusan zsúfoltabbá válik, mint például az izobutil-bromid esetében, a szubsztitúció lehetősége csökken, és az eliminációs reakcióút válik kedvezményezetté. A másik, eliminációt segítő tényező a bázis erőssége. A kevésbé bázisos benzoát szubsztráttal az izopropil-bromid 55%-ban szubsztitúciós reakcióba lép. Általában az ilyen típusú reakciók gáz és oldat fázisban is ugyanazokat a tendenciákat követik, bár az előbbiek az oldószer hatását kizárják.
Körforgalom mechanizmus szerkesztés
Egy 2008-as fejlemény felkeltette a kutatók érdeklődését, ez az SN2 körforgalom mechanizmus, melyet kloridionok és metil-jodid gáz fázisú reakciójában figyelték meg egy speciális eljárás, az úgynevezett keresztezett molekulasugaras képalkotás (crossed molecular beam imaging) segítségével. Amikor a kloridionok sebessége kellően nagy, az ütközés után termékként keletkező jodidionok energiája az előzetesen vártnál jóval alacsonyabb. Azt feltételezik, hogy az energiaveszteséget az okozza, hogy ilyenkor a metilcsoport a jódatom körül egy teljes kört tesz meg, mielőtt a tényleges reakció lejátszódna.[12][13][14]
Hivatkozások szerkesztés
- ↑ McMurry, John E. (1992), Organic Chemistry (3rd ed.), Belmont: Wadsworth, ISBN 0-534-16218-5
- ↑ Smith, Michael B. & March, Jerry (2007), Advanced Organic Chemistry: Reactions, Mechanisms, and Structure (6th ed.), New York: Wiley-Interscience, ISBN 0-471-72091-7, <https://books.google.com/books?id=JDR-nZpojeEC&printsec=frontcover>
- ↑ a b c Absence of SN1 Involvement in the Solvolysis of Secondary Alkyl Compounds, T. J. Murphy, J. Chem. Educ.; 2009; 86(4) pp 519-24; (Article) doi: 10.1021/ed041p678
- ↑ Relation of Steric orientation to Mechanism in Substitution Involving Halogen Atoms and Simple or Substituted Hydroxyl Groups, W. A. Cowdrey, E. D. Hughes, C. K. Ingold, S. Masterman, A. D. Scott, J. Chem. Soc.; 1937; 1252–1271. 10.1039/JR9370001252
- ↑ The 2-Adamantyl System, a Standard for Limiting Solvolysis in a Secondary Substrate J. L. Fry, C. J. Lancelot, L. K. M. Lam, J. M Harris, R. C. Bingham, D. J. Raber, R. E. Hill, P. v. R. Schleyer, J. Am. Chem. Soc.,; 1970; 92, pp 1240-42 (Article); doi: 10.1021/ja00478a031
- ↑ A Clarification of the Mechanism of Solvolysis of 2-Octyl Sulfonates. Stereochemical Considerations; H. Weiner, R. A. Sneen, J. Am. Chem. Soc.,; 1965; 87 pp 287-91; (Article) doi: 10.1021/ja01080a026
- ↑ A Clarification of the Mechanism of Solvolysis of 2-Octyl Sulfonates. Kinetic Considerations; H. Weiner, R. A. Sneen, J. Am. Chem. Soc.; 1965; 87 pp 292-96; (Article) doi: 10.1021/ja01080a027
- ↑ Homogeneous Hydrolysis and Alcoholysis of β-n-Octyl halides, E. D. Hughes, C. K. Ingold, S. Masterman, J. Chem. Soc.; 1937; pp 1196–1201; (Article) doi: 10.1039/JR9370001196
- ↑ Elimination Reactions Are Favored By Heat — Master Organic Chemistry. www.masterorganicchemistry.com . (Hozzáférés: 2018. április 13.)
- ↑ Gas Phase Studies of the Competition between Substitution and Elimination Reactions Scott Gronert Acc. Chem. Res.; 2003; 36(11) pp 848 - 857; (Article) doi:10.1021/ar020042n
- ↑ Az alkalmazott eljárás az elektrospray ionizációs technika, és mivel ennél a detektáláshoz töltéssel rendelkező reakciótermékre van szükség, a nukleofilre egy további – nem reakcióképes, és a másik aniontól jól elkülönített – szulfonát anion csoportot helyeztek. A szubsztitúciós és eliminációs termékek aránya meghatározható a megfelelő molekulaion csúcsaik relatív intenzitásából.
- ↑ Imaging Nucleophilic Substitution Dynamics J. Mikosch, S. Trippel, C. Eichhorn, R. Otto, U. Lourderaj, J. X. Zhang, W. L. Hase, M. Weidemüller, and R. Wester Science 11 January 2008 319: 183-186 doi:10.1126/science.1150238 (in Reports)
- ↑ PERSPECTIVES CHEMISTRY: Not So Simple John I. Brauman (11 January 2008) Science 319 (5860), 168. doi:10.1126/science.1152387
- ↑ Surprise From SN2 Snapshots Ion velocity measurements unveil additional unforeseen mechanism Carmen Drahl Chemical & Engineering News January 14, 2008 Volume 86, Number 2 p. 9 http://pubs.acs.org/cen/news/86/i02/8602notw1.html, video included
Fordítás szerkesztés
Ez a szócikk részben vagy egészben a SN2 reaction című angol Wikipédia-szócikk ezen változatának fordításán alapul. Az eredeti cikk szerkesztőit annak laptörténete sorolja fel. Ez a jelzés csupán a megfogalmazás eredetét és a szerzői jogokat jelzi, nem szolgál a cikkben szereplő információk forrásmegjelöléseként.