Vezikulum
A vezikulum lipid kettősréteggel körülvett folyadékból vagy citoplazmából álló, sejten belüli vagy kívüli szerkezet. A sejtmembránban történő szekréció (exocitózis), felvétel (endocitózis) és transzport során keletkezik, ahol liposzómáknak nevezik. 1 kettősréteg esetén a vezikulum egy-, több esetén többlamellás liposzóma.[1] A vezikulummembrán is lamellás fázisú a sejtmembránhoz hasonlóan, és a sejtbeli vezikulumok egyesülhetnek a sejtmembránnal tartalmuk sejten kívülre helyezéséhez. Ezenkívül más sejtszervecskékkel is egyesülhetnek.

Számos funkciójuk van. Mivel a citoszoltól elkülönül, a vezikulum belseje különbözhet a citoszol könnyezetétől. Így a vezikulumokat a sejtek anyagaik rendezésére használják. Részt vesznek az anyagcserében, a transzportban, a felhajtóerő-irányításban[2] és az ideiglenes tápanyag- és enzimtárolásban. Reakciókamraként is működhetnek.
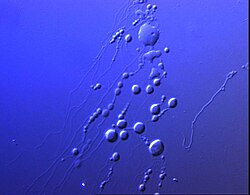
Oldószert (általában vizet) tartalmazó, amfifil molekulákból álló zárt szerkezet.[3]
A 2013-as orvosi Nobel-díjat James Rothman, Randy Schekman és Thomas Südhof megosztva kapták a vezikulumok szerkezetét és funkcióját, különösen élesztőben és emberben, beleértve a vezikulumok részeiről és azok elrendeződéséről szóló információt. A vezikulumdiszfunkció feltehetően közreműködhet az Alzheimer-kórban, a diabetes mellitusban, egyes nehezen kezelhető epilepsziaesetekben, egyes rákokban, immunológiai rendellenességekben és neurovascularis zavarokban.[4][5]
Vezikulumszerkezetek típusai
szerkesztésVakuólumok
szerkesztésA vakuólumok többnyire vizet tartalmazó sejtszervecskék.[6]
- A növényi sejtek nagy központi vakuólummal rendelkeznek a sejt közepén, ezt ozmoregulációra és tápanyagtárolásra használják.
- Egyes protiszták, különösen a csillósok kontraktilis vakuólumokkal rendelkeznek. Ezek vizet vesznek fel a citoplazmából, és kiviszik a sejtből az ozmózisnyomás miatti robbanás elkerüléséért.
Lizoszómák
szerkesztés- A lizoszóma a sejtemésztésben vesz részt. A táplálék a sejten kívülről bekerülhet a az emésztő űrbe endocitózissal. Ezek egyesülnek a részecskéket lebontó lizoszómákkal, lehetővé téve azok felhasználását. Ez a fagocitózis.
- A lizoszómák a hibás vagy sérült sejtszervecskéket is lebonthatják autofágia útján. Ekkor egyesülnek a hibás sejtszervecske membránjával, lebontva azt.
Szállító űröcskék
szerkesztés- A szállító vezikulumok a sejten belül mozgathatnak anyagokat, például fehérjéket a durva felszínű endoplazmatikus retikulumtól a Golgi-készülékig.
- A membránkötött és elválasztott fehérjék a durva endoplazmatikus retikulumon lévő riboszómák felszínén keletkeznek. Ezek legtöbbje a Golgi-készüléken érik végső helyszínük előtt, mely lehet lizoszóma, peroxiszóma vagy a sejten kívül is. E fehérjék a sejten belül szállító űröcskéken belül mozognak.
Elválasztó űröcskék
szerkesztésAz elválasztó űröcskék a sejtből elválasztandó anyagokat tartalmaznak. A sejteknek több okuk lehet az anyagok elválasztására, például a salakanyagok eltávolítása vagy a sejtfunkció. Nagyobb élőlényben egyes sejtek adott anyagok termelésére specializálódtak. Ezen anyagok elválasztó űröcskékben tárolódnak, és szükség esetén felszabadulnak.
Típusok
szerkesztés- A neurotranszmittereket tároló szinaptikus vezikulumok a neuronok preszinaptikus végein vannak. Ha az axonon jel érkezik, a neurotranszmittert felszabadítva egyesülnek a sejtmembránnal, így észlelheti a következő neuron receptora.
- Az állati endokrin szövetek hormonokat bocsátanak ki a véráramba. Ezeket elválasztó űröcskék tárolják. Példák erre a hasnyálmirigyben a Langerhans-szigetek. Ezek számos sejttípust tartalmaznak, melyeket az általuk termelt hormonok határoznak meg.
- Az elválasztó vezikulumok tartalmazzák a növények, protiszták, gombák, baktériumok és archeák sejtfalának, az állati sejtek extracelluláris mátrixának előállításához szükséges enzimeket.
- A baktériumok, archeák, gombák és paraziták membránvezikulumokat bocsátanak ki változó, de speciális méreg- és biokémiai jelzőanyagokkal, melyek a célsejtekbe kerülve a mikrobának előnyös folyamatokat indítanak, beleértve a gazdasejtek megtámadását és az azonos niche-ben versengő mikrobák elölését.[7]
Sejten kívüli űröcskék
szerkesztésA sejten kívüli űröcske (EV) lipid kettősréteggel határolt részecske, melyet minden domén készít, beleértve a komplex eukariótákat, a Gram-negatív és -pozitív baktériumokat, a mikobaktériumokat és a gombákat.[8][9]
Típusai
szerkesztés- A mikrovezikulumok közvetlenül a sejtmembránból válik le, átmérője 30 nm-től több mint 1 μm-ig terjedhet.[10]:Table 1). Lehetnek köztük nagy részecskék, például a haló sejtek által kibocsátott apoptotikus blebek,[10]:Table 1[11] egyes ráksejtek nagy onkoszómái vagy a fonálféreg-neuronok és egérszívizomsejtek kibocsátotta exoferek.[12]
- Exoszómák: sejten belüli eredetű membrános vezikulumok (átmérőjük 30-100 nm).[10]:Table 1
A különböző típusú EV-k sűrűség[10]:Table 1 (fokozatos differenciálcentrifugálással), méret vagy felszíni markerek alapján választhatók el.[13] Azonban az EV-altípusok méret- és sűrűségtartománya átfed egymással, az altípusra jellemző markerek sejtről sejtre határozandók meg. Így nehéz az adott EV keletkezésének útvonalát meghatározni, miután elhagyta a sejtet.[9]
Emberben az endogén EV-k feltehetően fontosak a koagulációban, a sejtbeli jelzésben és a salakanyag-kezelésben.[10] Fontosak lehetnek továbbá számos betegség, például a rák patofiziológiai folyamataiban.[14] Az EV-k fontosak lehetnek továbbá biomarkerek felfedezésében sejtbeli kommunikációban betöltött szerepük, könnyen hozzáférhető folyadékokba való kerülésük és a kibocsátó sejtekhez hasonló összetételük miatt.[15] A mezenchimális őssejtek EV-it, vagyis az őssejtszekretomot terápiás célokra használják és kutatják, főleg degeneratív, autoimmun vagy gyulladásos betegségekkel szemben.[16]
A Gram-negatív baktériumok a külső membrán leválasztásával termelnek EV-t, azonban az EV-k Gram-pozitív baktériumok, mikobaktériumok és gombák vastag sejtfalaiból való kikerülésének módja ismeretlen. Tartalmuk változó, lehet nukleinsav, toxin, lipoprotein és a mikrobák fiziológiája és patogenezise szempontjából fontos enzimek. A gazda-patogén interakciókban a Gram-negatív baktériumok kolonizációs niche-t kialakító EV-kat termelnek, ezek virulenciafaktorokat hordoznak és szállítanak, modulálva a gazda védekezését és válaszát.[17]
A cianobaktériumok folyamatosan termelnek fehérjéket, DNS-t és RNS-t tartalmazó vezikulumokat a nyílt tengerbe. A különböző baktériumok DNS-ét tartalmazók gyakoriak a parti és nyílt tengeri tengervízmintákban.[18]
Protosejtek
szerkesztésAz RNS-világ-hipotézis szerint az első önreplikáló genomok RNS-ből álltak, ezek RNS-replikáció katalízisére képes ribozimeket alkottak. Ezen elsődleges biológiai katalizátorok feltehetően zsírsavakból és hasonló amfifilekből álló membránnal rendelkező vezikulumokban (protosejt) lehettek.[19] Az RNS-templát-másolással történő templátirányított RNS-szintézist Adamata és Szostak mutatták be.[19]
Egyéb
szerkesztésGázvezikulumokat használnak az archeák, baktériumok és a plankton-mikroorganizmusok, feltehetően a függőleges mozgás gázmennyiség- és így felhajtóerő-szabályzással való irányítására vagy a maximális napfényhasználathoz való mozgásra. E vezikulumok általában citrom vgy hengeralakú fehérjecsövek;[20] átmérőjük határozza meg erejüket: a nagyobbak gyengébbek. A vezikulum átmérője határozza meg térfogatát és a felhajtóerő-biztosítás hatékonyságát is. A természetes kiválasztás a cianobaktériumokban a maximális átmérőjű stabil szerkezetű vezikulumokat részesítette előnyben. A fehérje a gázoknak permeábilis, a víznek nem, így ezek nem telnek meg vízzel.[2]
A mátrixvezikulumok az ECM-ben vannak. Elektronmikroszkóppal egymástól függetlenül fedezték fel 1967-ben H. Clarke Anderson[21] és Ermanno Bonucci.[22]
Keletkezés és transzport
szerkesztésVezikulumborítás és szállítómolekulák
szerkesztésA vezikulumborítás fehérjékből áll, melyek a donormembrán görbületét határozzák meg, kerek vezikulumot adva. E fehérjék transzmembrán receptorokhoz is kapcsolódhatnak. Ezek lehetővé teszik annak eldöntését, hogy mely anyag endocitózisa történik receptormediált endocitózissal vagy sejtbe való transzporttal.
Háromféle vezikulumborítás van, ezek a klatrin, a COPI és a COPII. Ezek típusai teszik lehetővé a vezikulumok elrendezését végső helyükre. Klatrinborítás a Golgi-készülék és a sejtmembrán, a Golgi-készülék és az endoszóma és a sejtmembrán és az endoszóma közt szállító vezikulumoknál van. COPI borítás a Golgi-készüléktől az ER-ig való retrográd transzport esetén van, COPII borítás az ER-től a Golgi-készülékig való anterográd transzport esetén.
A klatrinborítás felthetően a szabályzó G-proteinre válaszolva alakul ki. Az ADP-ribozilációs faktor (ARF) hatására alakul ki a fehérjeborítás.
Vezikulumkapcsolás
szerkesztésA SNARE felszíni fehérjék azonosítják a vezikulum tartalmát és a célmembrán komplementer SNARE-jeit, lehetővé téve a vezikulum és a cél fúzióját. Ezek feltehetően a vezikulummembránon vannak, a célmembránon lévő komplementerek a t-SNARE-ek.[23]
Gyakran a vezikulumokkal vagy célmembránokkal asszociált SNARE-eket Qa, Qb, Qc vagy R SNARE-ként sorolják be. A különböző SNARE-komplexek csoportjai különböző szöveeken és sejtbeli részekben találhatók. 36 humán izoforma ismert.[24]
A szabályzó Rab fehérjék vizsgálják a SNARE-csatlakozást. Ez szabályzó GTP-kötő fehérje, mely a komplementer SNARE-ek kötését elég hosszú ideig irányítja a megkötött GTP hidrolíziséhez és a vezikulum csatlakoztatásához.
A növényi SNARE-eket kevésbé tanulmányozták a gomba- és állati SNARE-eknél. Natasa Raihel ezzel kapcsolatban alapkutatásban vett részt, például Zheng et al. (1999)-ben, ahol ő és társai kimutatták, hogy az AtVTI1a fontos a Golgi-készülék⇄vakuólum transzportban.[25]
Vezikulumfúzió
szerkesztésKétféleképp történhet vezikulumfúzió: lehet teljes vagy átmeneti. A fúzióhoz a két membránnak 1,5 nm-nél közelebb kell lennie. Ehhez a vezikulumfelszíntől víznek kell távoznia. Ez energetikailag kedvezőtlen, ezért szükséges hozzá ATP, GTP és acetil-CoA. A fúziót a csírázással is összekapcsolták, innen a „csírázás és egyesülés” fogalma.[26]
A receptorműködés csökkentésében
szerkesztésA receptorként működő membránproteinek működését az ubikvitin csökkenti. A fent leírt módon endoszómához érve a vezikulumok az endoszómában vezikulumok keletkeznek, a bontásra szánt membránproteineket szállítva. Az endoszóma lizoszómává érésekor vagy azzal való egyesülésekor a vezikulumok lebomlanak. Enélkül a lizoszóma lumenjét csak a membránproteinek külső része érhetné el, és csak ez a rész bomlanék le.[27]
E vezikulumok miatt tekinthető az endoszóma többvezikulumos testnek. Keletkezésük módja nem teljesen ismert, szemben a fent leírt vezikulumokkal, a vezikulumok külső felszíne nem érintkezik a citoszollal.
Előállítás
szerkesztésIzolált vezikulumok
szerkesztésA membránvezikulumok előállítása a sejtmembránvizsgálati módszer. Miután az élő szövet szuszpenzióba kerül, egyes membránok kis zárt buborékokat alkotnak. A nagyobb sejttöredékek kis sebességű centrifugálással megszüntethetők, majd az ismert eredet (plazmalemma, tonoplasztisz stb.) frakciója precíz nagy sebességű centrifugálással izolálható. Ozmotikus sokkal a ideiglenesen felnyithatók a vezikulumok, feltölthetők a kívánt oldattal, ismét centrifugálhatók, és új oldatba helyezhetők. Ionoforokkal, például valinomicinnel az élő sejteken belülihez hasonló elektrokémiai gradiens hozható létre.
A vezikulumokat általában két kutatási típusban használják:
- Hormonokat és más fontos anyagokat specifikusan kötő membránreceptorok keresésére és izolálására.[28]
- Ionok vagy más anyagok transzportjának vizsgálatára adott típusú membránon keresztül.[29] Bár a transzport könnyebben vizsgálható patch clamppel, a vezikulumok izolálhatók azon esetben, ha a patch clamp nem használható.
Mesterséges vezikulumok
szerkesztésA mesterséges vezikulumok háromféle csoportba tartozhatnak méretük alapján: a kis egylamellás vezikulumok (SUV) mérete 20-100 nm, a nagy egylamellás vezikulumoké (LUV) 100-1000 nm, az óriás egylamellás vezikulumoké (GUV) 1-200 μm.[30] Az élő sejtek szállítóvezikulumaival azonos mérettartományba tartozó kisebb vezikulumokat gyakran használnak biokémiában és hasonló területekben. Ehhez homogén foszfolipid vezikulumszuszpenzió állítható elő extrúzióval, szonikációval[31] vagy foszfolipidoldat gyors injekciójával vizes pufferoldatba.[32] Így különböző foszfolipid-összetételű vizes vezikulumoldatok és különböző méretű vezikulumok állíthatók elő. A nagyobb szintetikus vezikulumokat, például a GUV-okat gyakran használják in vitro a sejtbiológiában sejtmembránok utánzására. E vezikulumok elég nagyok, hogy fluoreszcenciamikroszkóppal tanulmányozhatók legyenek. Számos módszer létezik a biológiai reagensek, például a fehérjeoldatok vezikulumokba zárására, így a GUV-ok ideális rendszerek a sejtfunkciók in vitro utánzására és vizsgálatára sejtszerű modellmembrán-környezetekben.[33] Ilyen módszerek még a mikrofolyadékos módszerek, mellyel sok állandó méretű vezikulum állítható elő.[34]
Jegyzetek
szerkesztés- ↑ Akbarzadeh A, Rezaei-Sadabady R, Davaran S, Joo SW, Zarghami N, Hanifehpour Y, Samiei M, Kouhi M, Nejati-Koshki K (2013. február 1.). „Liposome: classification, preparation, and applications”. Nanoscale Res Lett 8 (1), 102. o. DOI:10.1186/1556-276X-8-102. PMID 23432972.
- ↑ a b Walsby AE (1994. március 1.). „Gas vesicles”. Microbiological Reviews 58 (1), 94–144. o. DOI:10.1128/mmbr.58.1.94-144.1994. PMID 8177173.
- ↑ Slomkowski S, Alemán JV, Gilbert RG, Hess M, Horie K, Jones RG, Kubisa P, Meisel I, Mormann W, Penczek S, Stepto RF (2011). „Terminology of polymers and polymerization processes in dispersed systems (IUPAC Recommendations 2011)”. Pure and Applied Chemistry 83 (12), 2229–2259. o. [2013. október 20-i dátummal az eredetiből archiválva]. DOI:10.1351/PAC-REC-10-06-03. (Hozzáférés: 2023. november 13.)
- ↑ Nobel medical prize goes to 2 Americans, 1 German. CNN, 2005. október 19. (Hozzáférés: 2013. október 9.)
- ↑ 2013 Nobel Prize in Physiology or Medicine, press release 2013-10-07
- ↑ Matteo Figini, Daniel C. Alexander, Veronica Radanelli, Marina Grisoli, Giuseppe Baselli, Pierluigi Gambetti, Fabrizio Tagliavini, Alberto Bizzi (2014. november 29.). „Mathematical models for the diffusion magnetic resonance signal abnormality in patients with prion diseases”. Neuroimage Clin 2015 (7), 142–154. o. DOI:10.1016/j.nicl.2014.11.017. PMID 25610776. (Hozzáférés: 2023. november 14.)
- ↑ Deatherage BL, Cookson BT (2012. június 1.). „Membrane vesicle release in bacteria, eukaryotes, and archaea: a conserved yet underappreciated aspect of microbial life”. Infection and Immunity 80 (6), 1948–57. o. DOI:10.1128/IAI.06014-11. PMID 22409932.
- ↑ Yáñez-Mó M, Siljander PR, Andreu Z, Zavec AB, Borràs FE, Buzas EI, Buzas K, Casal E, Cappello F, Carvalho J, Colás E, Cordeiro-da Silva A, Fais S, Falcon-Perez JM, Ghobrial IM, Giebel B, Gimona M, Graner M, Gursel I, Gursel M, Heegaard NH, Hendrix A, Kierulf P, Kokubun K, Kosanovic M, Kralj-Iglic V, Krämer-Albers EM, Laitinen S, Lässer C, Lener T, Ligeti E, Linē A, Lipps G, Llorente A, Lötvall J, Manček-Keber M, Marcilla A, Mittelbrunn M, Nazarenko I, Nolte-'t Hoen EN, Nyman TA, O'Driscoll L, Olivan M, Oliveira C, Pállinger É, Del Portillo HA, Reventós J, Rigau M, Rohde E, Sammar M, Sánchez-Madrid F, Santarém N, Schallmoser K, Ostenfeld MS, Stoorvogel W, Stukelj R, Van der Grein SG, Vasconcelos MH, Wauben MH, De Wever O (2015). „Biological properties of extracellular vesicles and their physiological functions”. Journal of Extracellular Vesicles 4, 27066. o. DOI:10.3402/jev.v4.27066. PMID 25979354.
- ↑ a b Théry C, Witwer KW, Aikawa E, Alcaraz MJ, Anderson JD, Andriantsitohaina R, Antoniou A, Arab T, Archer F, Atkin-Smith GK, Ayre DC, Bach JM, Bachurski D, Baharvand H, Balaj L, Baldacchino S, Bauer NN, Baxter AA, Bebawy M, Beckham C, Bedina Zavec A, Benmoussa A, Berardi AC, Bergese P, Bielska E, Blenkiron C, Bobis-Wozowicz S, Boilard E, Boireau W, Bongiovanni A, Borràs FE, Bosch S, Boulanger CM, Breakefield X, Breglio AM, Brennan MÁ, Brigstock DR, Brisson A, Broekman ML, Bromberg JF, Bryl-Górecka P, Buch S, Buck AH, Burger D, Busatto S, Buschmann D, Bussolati B, Buzás EI, Byrd JB, Camussi G, Carter DR, Caruso S, Chamley LW, Chang YT, Chen C, Chen S, Cheng L, Chin AR, Clayton A, Clerici SP, Cocks A, Cocucci E, Coffey RJ, Cordeiro-da-Silva A, Couch Y, Coumans FA, Coyle B, Crescitelli R, Criado MF, D'Souza-Schorey C, Das S, Datta Chaudhuri A, de Candia P, De Santana EF, De Wever O, Del Portillo HA, Demaret T, Deville S, Devitt A, Dhondt B, Di Vizio D, Dieterich LC, Dolo V, Dominguez Rubio AP, Dominici M, Dourado MR, Driedonks TA, Duarte FV, Duncan HM, Eichenberger RM, Ekström K, El Andaloussi S, Elie-Caille C, Erdbrügger U, Falcón-Pérez JM, Fatima F, Fish JE, Flores-Bellver M, Försönits A, Frelet-Barrand A, Fricke F, Fuhrmann G, Gabrielsson S, Gámez-Valero A, Gardiner C, Gärtner K, Gaudin R, Gho YS, Giebel B, Gilbert C, Gimona M, Giusti I, Goberdhan DC, Görgens A, Gorski SM, Greening DW, Gross JC, Gualerzi A, Gupta GN, Gustafson D, Handberg A, Haraszti RA, Harrison P, Hegyesi H, Hendrix A, Hill AF, Hochberg FH, Hoffmann KF, Holder B, Holthofer H, Hosseinkhani B, Hu G, Huang Y, Huber V, Hunt S, Ibrahim AG, Ikezu T, Inal JM, Isin M, Ivanova A, Jackson HK, Jacobsen S, Jay SM, Jayachandran M, Jenster G, Jiang L, Johnson SM, Jones JC, Jong A, Jovanovic-Talisman T, Jung S, Kalluri R, Kano SI, Kaur S, Kawamura Y, Keller ET, Khamari D, Khomyakova E, Khvorova A, Kierulf P, Kim KP, Kislinger T, Klingeborn M, Klinke DJ, Kornek M, Kosanović MM, Kovács ÁF, Krämer-Albers EM, Krasemann S, Krause M, Kurochkin IV, Kusuma GD, Kuypers S, Laitinen S, Langevin SM, Languino LR, Lannigan J, Lässer C, Laurent LC, Lavieu G, Lázaro-Ibáñez E, Le Lay S, Lee MS, Lee YX, Lemos DS, Lenassi M, Leszczynska A, Li IT, Liao K, Libregts SF, Ligeti E, Lim R, Lim SK, Linē A, Linnemannstöns K, Llorente A, Lombard CA, Lorenowicz MJ, Lörincz ÁM, Lötvall J, Lovett J, Lowry MC, Loyer X, Lu Q, Lukomska B, Lunavat TR, Maas SL, Malhi H, Marcilla A, Mariani J, Mariscal J, Martens-Uzunova ES, Martin-Jaular L, Martinez MC, Martins VR, Mathieu M, Mathivanan S, Maugeri M, McGinnis LK, McVey MJ, Meckes DG, Meehan KL, Mertens I, Minciacchi VR, Möller A, Møller Jørgensen M, Morales-Kastresana A, Morhayim J, Mullier F, Muraca M, Musante L, Mussack V, Muth DC, Myburgh KH, Najrana T, Nawaz M, Nazarenko I, Nejsum P, Neri C, Neri T, Nieuwland R, Nimrichter L, Nolan JP, Nolte-'t Hoen EN, Noren Hooten N, O'Driscoll L, O'Grady T, O'Loghlen A, Ochiya T, Olivier M, Ortiz A, Ortiz LA, Osteikoetxea X, Østergaard O, Ostrowski M, Park J, Pegtel DM, Peinado H, Perut F, Pfaffl MW, Phinney DG, Pieters BC, Pink RC, Pisetsky DS, Pogge von Strandmann E, Polakovicova I, Poon IK, Powell BH, Prada I, Pulliam L, Quesenberry P, Radeghieri A, Raffai RL, Raimondo S, Rak J, Ramirez MI, Raposo G, Rayyan MS, Regev-Rudzki N, Ricklefs FL, Robbins PD, Roberts DD, Rodrigues SC, Rohde E, Rome S, Rouschop KM, Rughetti A, Russell AE, Saá P, Sahoo S, Salas-Huenuleo E, Sánchez C, Saugstad JA, Saul MJ, Schiffelers RM, Schneider R, Schøyen TH, Scott A, Shahaj E, Sharma S, Shatnyeva O, Shekari F, Shelke GV, Shetty AK, Shiba K, Siljander PR, Silva AM, Skowronek A, Snyder OL, Soares RP, Sódar BW, Soekmadji C, Sotillo J, Stahl PD, Stoorvogel W, Stott SL, Strasser EF, Swift S, Tahara H, Tewari M, Timms K, Tiwari S, Tixeira R, Tkach M, Toh WS, Tomasini R, Torrecilhas AC, Tosar JP, Toxavidis V, Urbanelli L, Vader P, van Balkom BW, van der Grein SG, Van Deun J, van Herwijnen MJ, Van Keuren-Jensen K, van Niel G, van Royen ME, van Wijnen AJ, Vasconcelos MH, Vechetti IJ, Veit TD, Vella LJ, Velot É, Verweij FJ, Vestad B, Viñas JL, Visnovitz T, Vukman KV, Wahlgren J, Watson DC, Wauben MH, Weaver A, Webber JP, Weber V, Wehman AM, Weiss DJ, Welsh JA, Wendt S, Wheelock AM, Wiener Z, Witte L, Wolfram J, Xagorari A, Xander P, Xu J, Yan X, Yáñez-Mó M, Yin H, Yuana Y, Zappulli V, Zarubova J, Žėkas V, Zhang JY, Zhao Z, Zheng L, Zheutlin AR, Zickler AM, Zimmermann P, Zivkovic AM, Zocco D, Zuba-Surma EK (2018). „Minimal information for studies of extracellular vesicles 2018 (MISEV2018): a position statement of the International Society for Extracellular Vesicles and update of the MISEV2014 guidelines”. Journal of Extracellular Vesicles 7 (1), 1535750. o. DOI:10.1080/20013078.2018.1535750. PMID 30637094.
- ↑ a b c d e van der Pol E, Böing AN, Harrison P, Sturk A, Nieuwland R (2012. július 1.). „Classification, functions, and clinical relevance of extracellular vesicles”. Pharmacological Reviews 64 (3), 676–705. o. DOI:10.1124/pr.112.005983. PMID 22722893.
- ↑ van der Pol E, Böing AN, Gool EL, Nieuwland R (2016. január 1.). „Recent developments in the nomenclature, presence, isolation, detection and clinical impact of extracellular vesicles”. Journal of Thrombosis and Haemostasis 14 (1), 48–56. o. DOI:10.1111/jth.13190. PMID 26564379.
- ↑ Melentijevic I, Toth ML, Arnold ML, Guasp RJ, Harinath G, Nguyen KC, Taub D, Parker JA, Neri C, Gabel CV, Hall DH, Driscoll M (2017. február 1.). „C. elegans neurons jettison protein aggregates and mitochondria under neurotoxic stress”. Nature 542 (7641), 367–371. o. DOI:10.1038/nature21362. PMID 28178240.
- ↑ Mateescu B, Kowal EJ, van Balkom BW, Bartel S, Bhattacharyya SN, Buzás EI, Buck AH, de Candia P, Chow FW, Das S, Driedonks TA, Fernández-Messina L, Haderk F, Hill AF, Jones JC, Van Keuren-Jensen KR, Lai CP, Lässer C, Liegro ID, Lunavat TR, Lorenowicz MJ, Maas SL, Mäger I, Mittelbrunn M, Momma S, Mukherjee K, Nawaz M, Pegtel DM, Pfaffl MW, Schiffelers RM, Tahara H, Théry C, Tosar JP, Wauben MH, Witwer KW, Nolte-'t Hoen EN (2017). „Obstacles and opportunities in the functional analysis of extracellular vesicle RNA - an ISEV position paper”. Journal of Extracellular Vesicles 6 (1), 1286095. o. DOI:10.1080/20013078.2017.1286095. PMID 28326170.
- ↑ Dhondt B, Rousseau Q, De Wever O, Hendrix A (2016. szeptember 1.). „Function of extracellular vesicle-associated miRNAs in metastasis”. Cell and Tissue Research 365 (3), 621–41. o. DOI:10.1007/s00441-016-2430-x. PMID 27289232.
- ↑ Dhondt B, Van Deun J, Vermaerke S, de Marco A, Lumen N, De Wever O, Hendrix A (2018. június 1.). „Urinary extracellular vesicle biomarkers in urological cancers: From discovery towards clinical implementation”. The International Journal of Biochemistry & Cell Biology 99, 236–256. o. DOI:10.1016/j.biocel.2018.04.009. PMID 29654900.
- ↑ Teixeira FG, Carvalho MM, Sousa N, Salgado AJ (2013. október 1.). „Mesenchymal stem cells secretome: a new paradigm for central nervous system regeneration?”. Cellular and Molecular Life Sciences 70 (20), 3871–82. o. DOI:10.1007/s00018-013-1290-8. PMID 23456256.
- ↑ Kuehn MJ, Kesty NC (2005. november 1.). „Bacterial outer membrane vesicles and the host-pathogen interaction”. Genes & Development 19 (22), 2645–55. o. DOI:10.1101/gad.1299905. PMID 16291643.
- ↑ Biller SJ, Schubotz F, Roggensack SE, Thompson AW, Summons RE, Chisholm SW (2014. január 1.). „Bacterial vesicles in marine ecosystems”. Science 343 (6167), 183–6. o. DOI:10.1126/science.1243457. PMID 24408433.
- ↑ a b Adamala K, Szostak JW (2013. november 29.). „Nonenzymatic template-directed RNA synthesis inside model protocells”. Science 342 (6162), 1098-1100. o. DOI:10.1126/science.1241888. PMID 24288333.
- ↑ Pfeifer F (2012. október 1.). „Distribution, formation and regulation of gas vesicles”. Nature Reviews. Microbiology 10 (10), 705–715. o. DOI:10.1038/nrmicro2834. PMID 22941504.
- ↑ Anderson HC (1967. október 1.). „Electron microscopic studies of induced cartilage development and calcification”. The Journal of Cell Biology 35 (1), 81–101. o. DOI:10.1083/jcb.35.1.81. PMID 6061727.
- ↑ Bonucci E (1967. szeptember 1.). „Fine structure of early cartilage calcification”. Journal of Ultrastructure Research 20 (1), 33–50. o. DOI:10.1016/S0022-5320(67)80034-0. PMID 4195919.
- ↑ (2011. október 1.) „Organization of SNAREs within the Golgi stack.”. Cold Spring Harbor Perspectives in Biology 3 (10), a005249. o. DOI:10.1101/cshperspect.a005249. PMID 21768609.
- ↑ Eliana V. Elias, Rodrigo Quiroga, Natalia Gottig, Hideki Nakanishi, Theodore E. Nash, Aaron Neiman, Hugo D. Lujan (2008. december 19.). „Characterization of SNAREs Determines the Absence of a Typical Golgi Apparatus in the Ancient Eukaryote Giardia lamblia”. J Biol Chem. DOI:10.1074/jbc.M806545200. PMID 18930915. (Hozzáférés: 2023. november 15.)
- ↑ (2017. április 28.) „Firmly Planted, Always Moving”. Annual Review of Plant Biology 68 (1), 1–27. o, Kiadó: Annual Reviews. DOI:10.1146/annurev-arplant-042916-040829. ISSN 1543-5008. PMID 27860488.
- ↑ Juan S. Bonifacino, Benjamin. S. Glick (2004. január 23.). „The mechanisms of vesicle budding and fusion”. Cell 116 (2), 153–166. o. DOI:10.1016/s0092-8674(03)01079-1. PMID 14744428. (Hozzáférés: 2023. november 15.)
- ↑ Katzmann DJ, Odorizzi G, Emr SD (2002. december 1.). „Receptor downregulation and multivesicular-body sorting”. Nature Reviews. Molecular Cell Biology 3 (12), 893–905. o. DOI:10.1038/nrm973. PMID 12461556.
- ↑ Sidhu VK, Vorhölter FJ, Niehaus K, Watt SA (2008. június 1.). „Analysis of outer membrane vesicle associated proteins isolated from the plant pathogenic bacterium Xanthomonas campestris pv. campestris”. BMC Microbiology 8, 87. o. DOI:10.1186/1471-2180-8-87. PMID 18518965.
- ↑ Scherer GG, Martiny-Baron G (1985). „K+/H+ exchange transport in plantmembranevesicles is evidence for K+ transport”. Plant Science 41 (3), 161–8. o. DOI:10.1016/0168-9452(85)90083-4.
- ↑ Walde P, Cosentino K, Engel H, Stano P (2010. május 1.). „Giant vesicles: preparations and applications”. ChemBioChem 11 (7), 848–65. o. DOI:10.1002/cbic.201000010. PMID 20336703.
- ↑ Barenholz Y, Gibbes D, Litman BJ, Goll J, Thompson TE, Carlson RD (1977. június 1.). „A simple method for the preparation of homogeneous phospholipid vesicles”. Biochemistry 16 (12), 2806–10. o. DOI:10.1021/bi00631a035. PMID 889789.
- ↑ Batzri S, Korn ED (1973. április 1.). „Single bilayer liposomes prepared without sonication”. Biochimica et Biophysica Acta (BBA) - Biomembranes 298 (4), 1015–9. o. DOI:10.1016/0005-2736(73)90408-2. PMID 4738145.
- ↑ Litschel T, Schwille P (2021. március 1.). „Protein Reconstitution Inside Giant Unilamellar Vesicles”. Annual Review of Biophysics 50, 525–548. o. DOI:10.1146/annurev-biophys-100620-114132. PMID 33667121.
- ↑ Sato Y, Takinoue M (2019. március 1.). „Creation of Artificial Cell-Like Structures Promoted by Microfluidics Technologies”. Micromachines 10 (4), 216. o. DOI:10.3390/mi10040216. PMID 30934758.
Fordítás
szerkesztésEz a szócikk részben vagy egészben a Vesicle (biology and chemistry) című angol Wikipédia-szócikk ezen változatának fordításán alapul. Az eredeti cikk szerkesztőit annak laptörténete sorolja fel. Ez a jelzés csupán a megfogalmazás eredetét és a szerzői jogokat jelzi, nem szolgál a cikkben szereplő információk forrásmegjelöléseként.