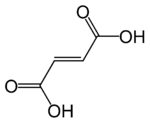
Fumársav
| Fumársav | |||
| |||

| |||
| IUPAC-név | (E)-buténdisav | ||
| Más nevek | transz-1,2-etiléndikarbonsav 2-buténdisav Allomaleinsav Boletinsav Zuzmósav (régies) | ||
| Kémiai azonosítók | |||
|---|---|---|---|
| CAS-szám | 110-17-8 | ||
| ATC kód | D05AX01 | ||
| |||
| Kémiai és fizikai tulajdonságok | |||
| Kémiai képlet | C4H4O4 | ||
| Moláris tömeg | 116,07 g/mol | ||
| Megjelenés | fehér kristály | ||
| Sűrűség | 1,635 g/cm³ | ||
| Olvadáspont | 287 °C | ||
| Savasság (pKa) | pKa1 = 3,03, pka2 = 4,44 | ||
| Veszélyek | |||
| Főbb veszélyek | Irritatív (Xi)[1] | ||
| R mondatok | R36[1] | ||
| S mondatok | (S2), S26[1] | ||
| Lobbanáspont | 273 °C[2] | ||
| Öngyulladási hőmérséklet | 375 °C[2] | ||
| LD50 | 9300 mg/kg (patkány, szájon át)[2] | ||
| Rokon vegyületek | |||
| Rokon karbonsavak | maleinsav borostyánkősav krotonsav | ||
| Rokon vegyületek | dimetil-fumarát vas(II)-fumarát | ||
| Ha másként nem jelöljük, az adatok az anyag standardállapotára (100 kPa) és 25 °C-os hőmérsékletre vonatkoznak. | |||
A fumársav (képlete: HO2CCH=CHCO2H) színtelen, szagtalan kristályos vegyület, telítetlen dikarbonsav-izomerpár egyike (transz izomer), a másik a maleinsav (cisz izomer). Gyümölcsös íze van.
Biológia szerkesztés
A fumársav megtalálható az orvosi füstikében (Fumaria officinalis), a Boletus fomentarius var. pseudo-igniarius gombában, zuzmókban és a gombák országába tartozó izlandi mohában (Cetraria islandica).
A fumársav, mely az almasav rokon vegyülete, ionizált formában (fumarát) előfordul a sejtekben a citromsavciklus folyamatában, amely cukrokból termel energiát ATP formájában. Az emberi bőr napfény hatására fumársavat termel.
Gyógyszer szerkesztés
A fumársav észtereit pszoriázis (bőrbetegség) kezelésében alkalmazzák, mert feltételezik, hogy a betegséget a bőr fumársavtermelésének hibája okozza. Kezdeti dózisként 60–105 mg-ot adnak naponta, amelyet fokozatosan egészen 1290 mg-ig emelhetnek. Mellékhatásként vese- és emésztési panaszok jelentkezhetnek, valamint bőrpír, de ezek főként túladagoláskor fordulnak elő. Hosszabb kezelés után csökkenhet a fehérvérsejtszám.
Élelmiszer szerkesztés
A fumársavat 1946 óta használják élelmiszer savasság-beállítóként, mivel nem mérgező. Italokban és sütőporokban használják, amelyeknek tisztasági követelményeknek kell megfelelniük.
Egyes esetekben a borkősavat és a citromsavat is helyettesítik vele: 1,36 g citromsav hatása megegyezik 0,91 g fumársav ízhatásával.
Gyakran előfordul élelmiszer-kiegészítőkben és adalékanyagokban is. Cukorkák előállításánál is felhasználják, az almasavhoz hasonlóan.
Kémia szerkesztés
Elsőként bróm-borostyánkősavból állították elő.[3] A hagyományos szintézisben a furfurált oxidálják nátrium-kloráttal, vanádium alapú katalizátor jelenlétében.[4] A fumársav kémiai tulajdonságaira a funkciós csoportjaiból következtethetünk. Mivel gyenge sav, diésztert alkot, a kettős kötés mentén addíciós reakciókban vehet részt, és kitűnő dienofil.
Más felhasználás szerkesztés
A fumársavat poliészter gyanták és cukoralkoholok gyártásánál valamint színezékek pácolásához is felhasználják.
Biztonság szerkesztés
Tökéletlen égéskor a fumársav maleinsav-anhidriddé alakulhat, ami irritáló vegyület.
Jegyzetek szerkesztés
- ↑ a b c A fumársav (ESIS)[halott link]
- ↑ a b c A fumársav vegyülethez tartozó bejegyzés az IFA GESTIS adatbázisából. A hozzáférés dátuma: 2010. november 1. (JavaScript szükséges) (angolul)
- ↑ Volhard, J. "Darstellung von Maleïnsäureanhydrid" Justus Liebig's Annalen der Chemie 1892, volume 268, page 255-6. DOI: 10.1002/jlac.18922680108
- ↑ Milas, N. A. "Fumaric Acid" Organic Synthesis 1943, Collective Volume 2, page 302. http://www.orgsyn.org/orgsyn/pdfs/CV2P0302.pdf
További információk szerkesztés
| A citromsavciklus anyagcsere-útvonala | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||